

La vida media o período radiactivo de un isótopo radiactivo es el tiempo necesario para que la mitad de los núcleos de una muestra se desintegren. Es una cantidad característica de un núcleo inestable y una medida probabilística de su estabilidad. La vida media es independiente de la cantidad de material o de las condiciones externas (temperatura, presión, etc.) porque la desintegración radiactiva es un proceso puramente cuántico, gobernado por las leyes de la mecánica cuántica.
Una vida media corta significa una desintegración rápida (elemento muy inestable). Una vida media larga indica un elemento más estable.
No, no todos los elementos químicos tienen una vida media medible, porque algunos isótopos son estables. Por ejemplo, el carbono-12 (12C), el oxígeno-16 (16O) o el hierro-56 (56Fe) no se desintegran espontáneamente, incluso en escalas de tiempo comparables a la edad del Universo. Por otro lado, los elementos radiactivos como el uranio, el torio o el polonio poseen una o más formas inestables (isótopos) con vidas medias que varían desde microsegundos hasta miles de millones de años.
El período radiactivo, a menudo denotado \( T_{1/2} \)), de un elemento químico (o más precisamente de un nucleido radiactivo) es, por lo tanto, el tiempo necesario para que la mitad de los núcleos de una muestra dada se desintegren espontáneamente. Es una medida de la estabilidad nuclear.
Para una muestra que contiene \( N_0 \) núcleos en el tiempo \( t = 0 \), la ley de decaimiento radiactivo es: \( N(t) = N_0 \cdot e^{-\lambda t} \)
La vida media \( T_{1/2} \) está relacionada con \( \lambda \) por: \( T_{1/2} = \frac{\ln(2)}{\lambda} \)
| Elemento | Isótopo | Vida Media (segundos) | Vida Media (Forma Legible) |
|---|---|---|---|
| Polonio | Po-212 | 0.0000003 | 0.3 µs |
| Livermorio | Lv-293 | 0.061 | 61 ms |
| Californio | Cf-251 | 0.9 | 0.9 s |
| Francio | Fr-223 | 1320 | 22 min |
| Tecnecio | Tc-99m | 21600 | 6 h |
| Yodo | I-131 | 693,728 | 8.02 d |
| Cobalto | Co-60 | 166,824,000 | 5.27 años |
| Hidrógeno | Tritio | 388,435,680 | 12.32 años |
| Carbono | C-14 | 180,622,080,000 | 5730 años |
| Plutonio | Pu-239 | 760,585,760,000 | 24,100 años |
| Uranio | U-234 | 7,740,138,000,000 | 245,500 años |
| Uranio | U-235 | 22,174,070,000,000 | 703 millones de años |
| Uranio | U-238 | 141,379,620,000,000 | 4.468 mil millones de años |
| Torio | Th-232 | 443,538,150,000,000 | 14.05 mil millones de años |
| Telurio | Te-128 | 6.945×10²⁴ | 2.2×10²⁴ s (~7×10¹⁶ años) |
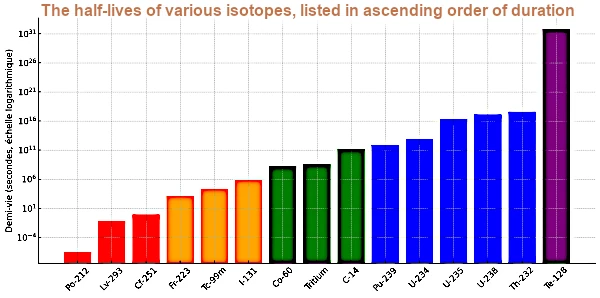
Este gráfico muestra las vidas medias de los isótopos seleccionados, ordenados en orden creciente. La escala logarítmica permite visualizar las enormes diferencias, que van desde microsegundos hasta más de 10²⁴ segundos.