

A meia-vida ou período radioativo de um isótopo radioativo é o tempo necessário para que metade dos núcleos de uma amostra se desintegre. É uma grandeza característica de um núcleo instável e uma medida probabilística de sua estabilidade. A meia-vida é independente da quantidade de material ou das condições externas (temperatura, pressão, etc.), pois a desintegração radioativa é um processo puramente quântico, governado pelas leis da mecânica quântica.
Uma meia-vida curta significa uma desintegração rápida (elemento muito instável). Uma meia-vida longa indica um elemento mais estável.
Não, nem todos os elementos químicos têm uma meia-vida mensurável, porque alguns isótopos são estáveis. Por exemplo, o carbono-12 (12C), o oxigênio-16 (16O) ou o ferro-56 (56Fe) não se desintegram espontaneamente, mesmo em escalas de tempo comparáveis à idade do Universo. Por outro lado, elementos radioativos como o urânio, o tório ou o polônio possuem uma ou mais formas instáveis (isótopos) com meias-vidas variando de microsegundos a bilhões de anos.
O período radioativo, muitas vezes denotado \( T_{1/2} \)), de um elemento químico (ou mais precisamente de um nuclídeo radioativo) é, portanto, o tempo necessário para que metade dos núcleos de uma amostra dada se desintegre espontaneamente. É uma medida da estabilidade nuclear.
Para uma amostra contendo \( N_0 \) núcleos no tempo \( t = 0 \), a lei de decaimento radioativo é: \( N(t) = N_0 \cdot e^{-\lambda t} \)
A meia-vida \( T_{1/2} \) está relacionada a \( \lambda \) por: \( T_{1/2} = \frac{\ln(2)}{\lambda} \)
| Elemento | Isótopo | Meia-Vida (segundos) | Meia-Vida (Forma Legível) |
|---|---|---|---|
| Polônio | Po-212 | 0.0000003 | 0.3 µs |
| Livermório | Lv-293 | 0.061 | 61 ms |
| Califórnio | Cf-251 | 0.9 | 0.9 s |
| Frâncio | Fr-223 | 1320 | 22 min |
| Tecnécio | Tc-99m | 21600 | 6 h |
| Iodo | I-131 | 693,728 | 8.02 d |
| Cobalto | Co-60 | 166,824,000 | 5.27 anos |
| Hidrogênio | Trítio | 388,435,680 | 12.32 anos |
| Carbono | C-14 | 180,622,080,000 | 5730 anos |
| Plutônio | Pu-239 | 760,585,760,000 | 24,100 anos |
| Urânio | U-234 | 7,740,138,000,000 | 245,500 anos |
| Urânio | U-235 | 22,174,070,000,000 | 703 milhões de anos |
| Urânio | U-238 | 141,379,620,000,000 | 4.468 bilhões de anos |
| Tório | Th-232 | 443,538,150,000,000 | 14.05 bilhões de anos |
| Telúrio | Te-128 | 6.945×10²⁴ | 2.2×10²⁴ s (~7×10¹⁶ anos) |
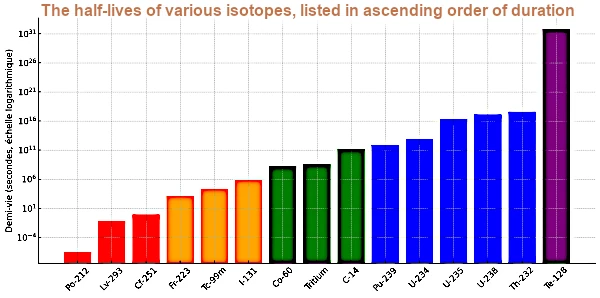
Este gráfico mostra as meias-vidas dos isótopos selecionados, classificados em ordem crescente. A escala logarítmica permite visualizar as enormes diferenças, que vão de microsegundos a mais de 10²⁴ segundos.