

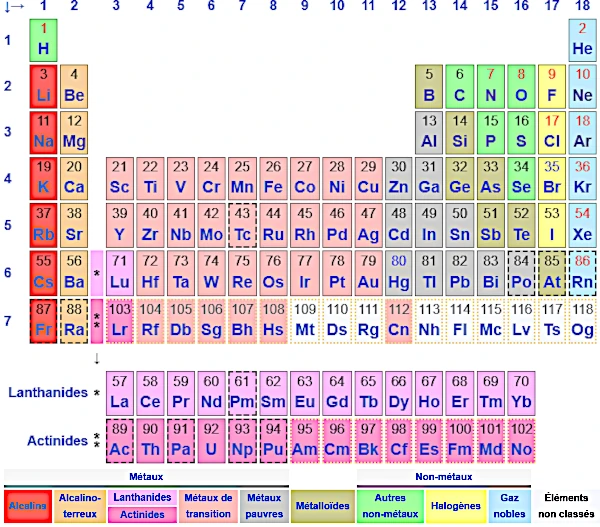
La Tabla Periódica de los Elementos Químicos, una de las herramientas más importantes en química, fue desarrollada por Dmitri Mendeléiev (1834-1907) en 1869. Su versión original clasificaba los 63 elementos conocidos en ese momento por masa atómica creciente y resaltaba la periodicidad de sus propiedades químicas. La gran innovación de Mendeléiev fue dejar espacios en blanco para elementos desconocidos en su época, cuyas propiedades predijo con notable precisión.
| Elemento | Símbolo | N° Atómico | Descubrimiento | Usos Modernos |
|---|---|---|---|---|
| Helio | He | 2 | 1868 (espectroscopia solar) | Globos, resonancia magnética, soldadura |
| Galio | Ga | 31 | 1875 | Semiconductores (chips electrónicos) |
| Germanio | Ge | 32 | 1886 | Fibras ópticas, lentes infrarrojas |
| Radio | Ra | 88 | 1898 (Pierre y Marie Curie) | Antiguamente en medicina (radioterapia) |
| Neón | Ne | 10 | 1898 | Iluminación (carteles luminosos) |
| Plutonio | Pu | 94 | 1940 | Energía nuclear (civil y militar) |
| Tecnecio | Tc | 43 | 1937 (1er elemento artificial) | Medicina nuclear (escáneres) |
| Francio | Fr | 87 | 1939 | Investigación fundamental (muy raro) |
| Uranio | U | 92 | 1789 (pero propiedades desconocidas) | Centrales nucleares, armamento |
| Platino | Pt | 78 | Conocido pero no estudiado | Catalizadores automotrices, joyería |
Mendeléiev había predicho con notable precisión las propiedades del galio (que llamaba "eka-aluminio"), del germanio ("eka-silicio") y del escandio ("eka-boro"). Estos descubrimientos posteriores validaron su tabla periódica.
La tabla moderna organiza los 118 elementos conocidos (hasta la fecha) según su número atómico (número de protones) y sus propiedades químicas recurrentes. Se compone de:
Los elementos se clasifican en tres grandes categorías:
Ciertos grupos tienen propiedades químicas particularmente similares:
Los elementos más allá del uranio (número atómico > 92) son generalmente sintéticos, producidos en laboratorio. A menudo son muy inestables y se desintegran rápidamente por radioactividad.