

En la naturaleza, toda la materia se concentra en la energía de masa de núcleos 100,000 veces más pequeños que un átomo, pero miles de veces más pesados que todos sus electrones.
En la materia, muchos núcleos atómicos son estables y su estado permanece indefinidamente igual. Un isótopo es estable cuando tiene un número armonioso de protones y neutrones. Por otro lado, muchos núcleos son inestables porque tienen demasiados protones o neutrones, o ambos. Los físicos han identificado poco menos de 300 isótopos estables y cerca de 3,000 inestables. Si los núcleos son inestables, es debido a la barrera de Coulomb, que establece una competencia entre la fuerza de repulsión electrostática entre protones y la fuerza nuclear atractiva entre neutrones y protones. Por eso los núcleos deben incorporar cada vez más neutrones a medida que crecen.
Todos los núcleos de materia buscan una estabilidad energética frugal. Así, para regresar a un estado estable, deben transformarse expulsando energía en forma de masa o radiación (E=mc^2). A esto se le llama radiactividad.
Este fenómeno de radiactividad natural está presente en toda la materia, tanto en minerales como en nuestros alimentos (la Comunidad Europea ha establecido límites para la radiactividad en los alimentos) e incluso en nuestros cuerpos (debido a la presencia de carbono-14 y potasio-40).
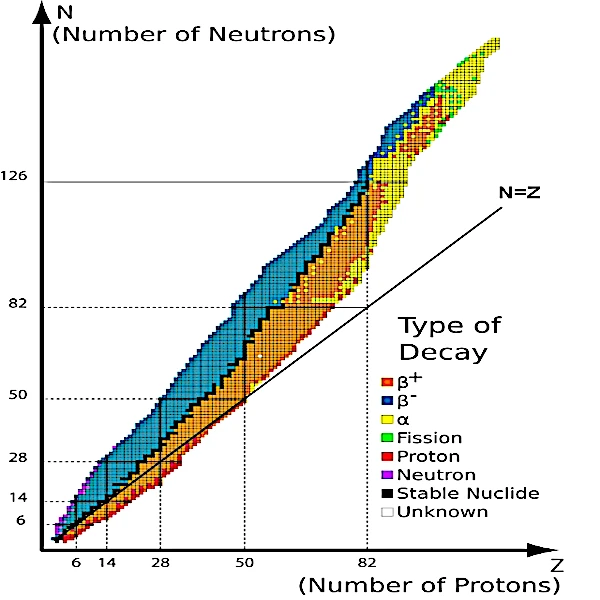
• Cuando se representan todos los isótopos conocidos en un gráfico (imagen arriba) por su número de protones (Z) y su número de neutrones (N), se observa que todos los isótopos estables (puntos negros) están agrupados alrededor de una línea. Esta línea está en el fondo de un valle llamado "valle de estabilidad".
Los núcleos inestables se distribuyen en los flancos del valle a ambos lados de esta línea negra que representa el río de materia estable que fluye en el fondo del valle. Cuanto más inestables son los núcleos, más altos se encuentran en el valle. Así, en este valle, el camino más corto para alcanzar la estabilidad es descender al fondo del valle.
• Los nucleidos en el flanco izquierdo del valle (en azul en la imagen), con exceso de neutrones en comparación con su número de protones, encuentran estabilidad a través de una cascada de desintegraciones β- con la emisión de electrones y neutrinos, que les permite descender gradualmente por las pendientes del valle.
• Los nucleidos en el flanco derecho del valle (en naranja), con exceso de protones, encuentran estabilidad a través de una cascada de desintegraciones β+ con la emisión de positrones y neutrinos.
• Los nucleidos en la pequeña cresta izquierda del valle (en púrpura) en el borde exterior de la zona azul, encuentran estabilidad a través de la emisión de neutrones; el núcleo mantiene el mismo número atómico (Z) pero su masa atómica disminuye.
• Los nucleidos situados en la pequeña cresta derecha del valle (en rojo) en el borde exterior de la zona naranja, encuentran estabilidad a través de la emisión de protones; el número atómico (Z) y la masa atómica del núcleo disminuyen.
• En el caso de núcleos muy pesados, interviene la fisión. Los nucleidos, más allá de la línea de isótopos estables (en verde claro), encuentran estabilidad mediante la división del núcleo en dos núcleos más ligeros con la emisión de uno o más neutrones.
• Los nucleidos de alta masa atómica (en amarillo) sufren una desintegración α a menudo acompañada de la emisión de fotones de alta energía o rayos gamma. Si la pendiente es demasiado alta, las desintegraciones β se intercalan entre las desintegraciones α. Se requiere una cascada de desintegraciones radiactivas para alcanzar el fondo del valle.
• Finalmente, los núcleos particularmente estables tienen un cierto número de nucleones (2, 8, 20, 28, 50, 82 y 126) que corresponden al modelo en capas del núcleo atómico (niveles de energía cuantificados basados en el principio de exclusión de Pauli). Estos números llamados mágicos están marcados a lo largo de los escalones de la curva negra. Los núcleos que tienen tanto un número mágico de protones como de neutrones y un número de protones igual al número de neutrones se denominan doblemente mágicos porque son muy estables.
Este es el caso del plomo-208, que consta de 82 protones y 126 neutrones, y del calcio-48, que consta de 20 protones y 28 neutrones.
• Las discontinuidades en la curva negra en neutrones (19, 21, 35, 39, 45, 84, 115 y 123) y en protones (43 y 61) corresponden a casos en los que no hay núcleos estables con estas cantidades de nucleones.
El valle de estabilidad contiene alrededor de 3,000 nucleidos observados, estables, inestables y muy inestables. Pero no conocemos los límites de estabilidad (líneas de goteo) de los nucleidos. Para los protones (número máximo de protones), se conoce relativamente a través de la tabla de Mendeleev. Para los neutrones (número máximo de neutrones), los límites de estabilidad solo se conocen para los primeros elementos, desde el hidrógeno hasta el oxígeno-15. Por ejemplo, para Z=8, el número máximo de neutrones es 16, haciendo que el oxígeno-24 sea el isótopo más pesado posible del oxígeno. El alcance completo del valle de estabilidad sigue siendo desconocido y parece que lo que queda por descubrir es enorme.
N.B.:
El núcleo del átomo está compuesto por protones y neutrones. Los átomos del mismo elemento químico tienen el mismo número de protones pero pueden tener un número diferente de neutrones; estos son los isótopos. Los átomos estables no sufren desintegración radiactiva.