

Dans la nature, toute la matière se retrouve concentrée dans l'énergie de masse des noyaux 100000 fois plus petits que l'atome, mais des milliers de fois plus lourds que l'ensemble de leurs électrons.
Dans la matière de nombreux noyaux d'atomes sont stables et leur état reste indéfiniment identique. Un isotope est stable lorsqu'il comporte un nombre harmonieux de protons et de neutrons. Par contre beaucoup de noyaux sont instables car ils possèdent trop de protons ou de neutrons ou trop des deux. Les physiciens ont identifié un peu moins de 300 isotopes stables et près de 3 000 instables. Si les noyaux sont instables c'est à cause de la barrière coulombienne qui établit une compétition entre la force de répulsion électrostatique entre les protons et la force nucléaire attractive entre les neutrons et les protons. C'est pourquoi les noyaux doivent intégrer de plus en plus de neutrons au fur et à mesure qu'ils grossissent.
Tous les noyaux de la matière cherchent une stabilité énergétique parcimonieuse. Ainsi pour revenir vers un état stable, ils doivent se transformer en expulsant de l'énergie sous forme de masse ou de rayonnements (E=mc2). C'est ce que l'on appelle la radioactivité.
Ce phénomène de radioactivité naturelle est en œuvre partout dans la matière, aussi bien dans les minéraux que dans notre alimentation (la Communauté européenne a fixé des doses de radioactivité à ne pas dépasser dans les aliments) et même dans notre corps (dû à la présence de carbone 14 et de potassium 40).
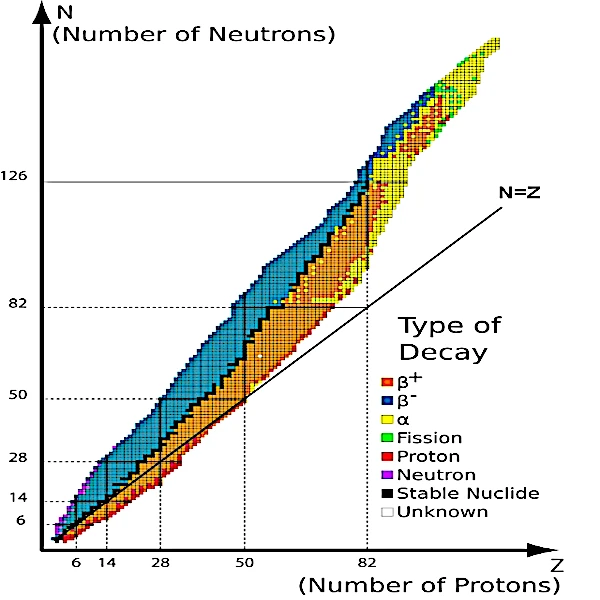
• Lorsque l'on représente tous les isotopes connus sur un graphe (image ci-dessus) par leur nombre de protons (Z) et leur nombre de neutrons (N), on constate que tous les isotopes stables (points noirs) sont regroupés autour d'une ligne. Cette ligne est au creux d'une vallée nommée "vallée de stabilité".
Les noyaux instables se répartissent sur les flancs de la vallée de part et d'autre de cette ligne noire représentant le fleuve de matière stable coulant au fond de la vallée. Plus les noyaux sont instables et plus il se situent haut dans la vallée. Ainsi, dans cette vallée, le plus court chemin pour rejoindre la stabilité est de descendre au fond de la vallée.
• Les nucléides sur le flanc gauche de la vallée (en bleu sur l'image), excédentaires en neutrons en comparaison de leur nombre de protons, retrouvent la stabilité par une cascade de désintégrations β- avec émission d'électrons et de neutrinos qui leur permet de descendre petit à petit les pentes de la vallée.
• Les nucléides sur le flanc droit de la vallée (en orange), excédentaires en protons, retrouvent la stabilité par une cascade de désintégrations β+ avec émission de positons et de neutrinos.
• Les nucléides sur la crête gauche peu étendue de la vallée (en violet) à la limite périphérique de la zone bleue, retrouvent la stabilité par émission de neutrons, le noyau garde le même numéro atomique (Z) mais sa masse atomique diminue.
• Les nucléides situés sur la crête droite peu étendue de la vallée (en rouge) à la limite périphérique de la zone orange, retrouvent la stabilité par émission de protons, le numéro atomique (Z) et la masse atomique du noyau diminuent.
• Du côté des noyaux très lourds, c'est la fission qui va intervenir. Les nucléides, au-delà de la ligne des isotopes stables (en vert pâle), retrouvent la stabilité par la division du noyau en deux noyaux plus légers avec émission d'un ou plusieurs neutrons.
• Les nucléides de masse atomique élevée (en jaune) subissent une désintégration α souvent accompagnée de l'émission de photons de haute énergie ou rayons gamma. Si la pente est trop haute alors des désintégrations β s'intercalent entre les désintégrations α. Une cascade de désintégrations radioactives est nécessaire pour atteindre le fond de la vallée.
• Enfin les noyaux particulièrement stables possèdent un certain nombre de nucléons (2, 8, 20, 28, 50, 82 et 126) qui correspondent au modèle en couches du noyau atomique (niveaux d'énergie quantifiés fondé sur le principe d'exclusion de Pauli). Ces nombres dits magiques sont repérés suivant les marches d'escalier de la courbe noire. Les noyaux qui ont à la fois un nombre magique de protons et de neutrons et un nombre de protons égal au nombre de neutrons sont dits doublement magiques car très stables.
C'est le cas du plomb 208 qui est constitué de 82 protons et 126 neutrons et du calcium 48, constitué de 20 protons et 28 neutrons.
• Les discontinuités de la courbe noire en neutrons (19, 21, 35, 39, 45, 84, 115 et 123) et en protons (43 et 61) correspondent aux cas où il n'y a aucun noyau stable avec ces quantités de nucléons.
La vallée de la stabilité contient environ 3000 nucléides observés, stables, instables et très instables. Mais nous ne connaissons pas les limites de stabilité (drip lines) des nucléides. Pour les protons (nombre maximum de protons) elle est relativement connue à travers le tableau de Mendeleïev. Pour les neutrons (nombre maximum de neutrons) les limites de stabilité ne sont connues que pour les premiers éléments, de l'hydrogène à l'oxygène 15. Par exemple, pour Z=8, le nombre maximal de neutrons est 16, donnant l'oxygène 24 comme l'isotope de l'oxygène le plus lourd possible. L'étendue complète de la vallée de la stabilité reste inconnue et il semble que ce qui reste à découvrir soit énorme.
N.B.: Le noyau de l'atome est constitué de protons et neutrons. Les atomes d'un même élément chimique ont le même nombre de protons mais peuvent avoir un nombre de neutrons différent, ce sont les isotopes. Les atomes stables ne subissent pas de désintégration radioactive.