

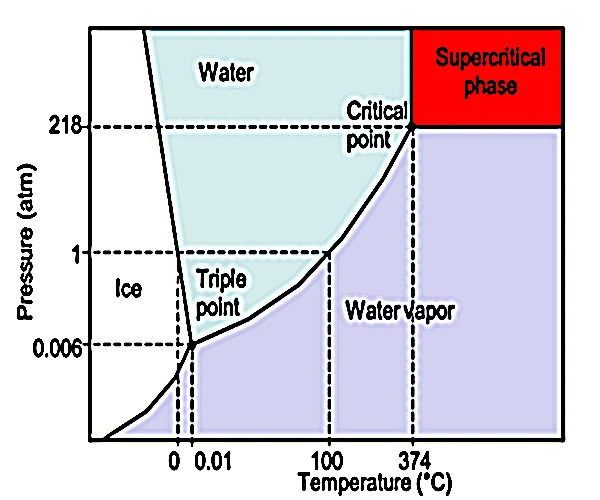
L’état supercritique de l’eau, atteint à une température de 374 °C et une pression de 22,06 MPa (≈217,8 atm), est un domaine thermodynamique dans lequel l’eau ne se distingue plus entre liquide et gaz. Dans cette zone, elle possède à la fois la densité d’un liquide et la diffusivité d’un gaz. Ce comportement hybride ouvre la voie à des propriétés physiques et chimiques uniques, la rendant très réactive, excellente pour dissoudre des substances organiques et inorganiques, et largement utilisée en géochimie, dans les procédés industriels, et même dans l'exploration des conditions prébiotiques.
Contrairement à l’eau liquide ou vapeur, l’eau supercritique présente des fluctuations de densité importantes à petite échelle, ce qui modifie les constantes diélectriques, la solvatation ionique et les mécanismes de transport thermique. Elle peut dissoudre des sels comme un liquide mais se comporter comme un gaz pour des espèces non polaires. Sa conductivité thermique est élevée, sa viscosité faible, et sa tension de surface est nulle. Ces caractéristiques en font un excellent fluide de travail ou un solvant vert dans des procédés de chimie durable.
L’état supercritique de l’eau ne peut exister qu’à des pressions supérieures à 217 atm et des températures au-delà de 374 °C. Ces conditions sont naturellement réunies dans certains environnements géothermiques profonds, notamment dans la croûte océanique et à proximité des chambres magmatiques. On en trouve notamment dans les zones suivantes :
Ces environnements extrêmes sont d’un intérêt majeur tant pour la recherche fondamentale (origine de la vie, extrêmophiles, minéralisation) que pour les technologies émergentes de géoénergie.
On retrouve l’eau supercritique dans divers domaines :
L’état supercritique de l’eau aurait pu jouer un rôle dans l’origine de la vie sur Terre. Dans les environnements hydrothermaux profonds, l’eau supercritique aurait favorisé des réactions organiques complexes, précurseurs à l’apparition des premières molécules biologiques. De plus, les propriétés exceptionnelles de solvatation et de catalyse ont pu servir de support au développement de chimies prébiotiques en surface ou dans la croûte terrestre.
| Propriété | Liquide | Vapeur | Supercritique |
|---|---|---|---|
| Densité (kg/m³) | 1000 | 0.6 | 200-500 |
| Viscosité (μPa·s) | 890 | 13 | 100-300 |
| Constante diélectrique | ≈80 | ≈1.0 | ≈10-20 |
| Solubilité des sels | Forte | Nulle | Moyenne à forte (variable) |
| Tension de surface | 72 mN/m | Nulle | Nulle |
Source : NIST Chemistry WebBook, ScienceDirect - Supercritical water oxidation.