

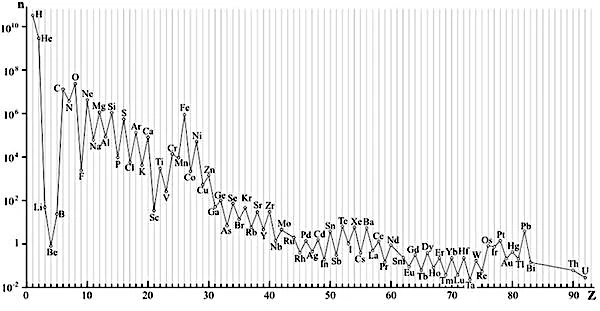
Parce que ces deux éléments sont les seuls à avoir été produits en quantité massive lors de la nucléosynthèse primordiale, dans les trois premières minutes qui ont suivi le Big Bang, il y a 13,8 milliards d'années. À ce moment-là, l'Univers en refroidissement a permis aux premiers protons et neutrons de s'assembler pour former environ 75 % d'hydrogène et 25 % d'hélium, avec seulement des traces infimes de lithium et de béryllium. Tous les autres éléments du tableau périodique – le carbone qui constitue nos corps, l'oxygène que nous respirons, le fer de nos globules rouges – ont été forgés bien plus tard, dans le cœur des étoiles par fusion nucléaire, puis dispersés dans l'espace par l'explosion violente des supernovae. La chimie de l'Univers est donc une histoire en deux temps: une composition initiale héritée du Big Bang, puis un enrichissement progressif par des générations successives d'étoiles, faisant de nous, au sens littéral, des "poussières d'étoiles".
Dans les premiers instants qui ont suivi le Big Bang, il y a environ 13,8 milliards d'années, l'Univers était une soupe de quarks et de gluons d'une densité et d'une température inimaginables. En se refroidissant, les premiers protons et neutrons se sont assemblés. Pendant les trois premières minutes, le cosmos a été le théâtre d'une synthèse nucléaire primordiale fulgurante. Le résultat de cette alchimie originelle est d'une simplicité absolue: environ 75 % d'hydrogène (¹H) et 25 % d'hélium (⁴He), avec des traces infimes de lithium et de béryllium.
Cet héritage initial, cette abondance primordiale, est la partition de base sur laquelle toute l'histoire cosmique va s'écrire. Aucun élément plus lourd que le lithium n'a pu émerger de cette époque. Pour créer le carbone, l'oxygène, le fer et tous les atomes qui constituent aujourd'hui les planètes, les océans et nos propres corps, il a fallu attendre la naissance, la vie et la mort violente des premières étoiles. Margaret Burbidge (1919-2020), astrophysicienne pionnière, a profondément marqué l’étude de la formation des éléments chimiques au sein des étoiles et de la structure des galaxies. Grâce à ses recherches, nous savons désormais que nous sommes, au sens littéral, composés de "poussières d'étoiles".
| Élément | Symbole | Abondance relative (atomes) (normalisée à 10⁶ atomes de Si) | Rapport de masse (fraction en %) | Principaux sites de production |
|---|---|---|---|---|
| Hydrogène | H | \( 4.0 \times 10^{10} \) | ~ 71 % | Big Bang (nucléosynthèse primordiale) |
| Hélium | He | \( 3.0 \times 10^{9} \) | ~ 27 % | Big Bang, fusion stellaire |
| Oxygène | O | \( 2.2 \times 10^{7} \) | ~ 0.9 % | Étoiles massives (fusion C, Ne, O), supernovae |
| Carbone | C | \( 1.0 \times 10^{7} \) | ~ 0.3 % | Étoiles de faible masse (processus triple alpha), étoiles massives |
| Néon | Ne | \( 1.8 \times 10^{6} \) | ~ 0.1 % | Étoiles massives (fusion du carbone) |
| Azote | N | \( 6.2 \times 10^{5} \) | ~ 0.09 % | Étoiles de faible masse (processus CNO), étoiles massives |
| Silicium | Si | \( 1.0 \times 10^{6} \) | ~ 0.07 % | Étoiles massives (fusion de l'oxygène, fusion du silicium) |
| Magnésium | Mg | \( 1.0 \times 10^{6} \) | ~ 0.06 % | Étoiles massives (fusion du néon et du carbone) |
| Fer | Fe | \( 8.3 \times 10^{5} \) | ~ 0.12 % | Supernovae (effondrement de cœur), supernovae de type Ia |
| Soufre | S | \( 4.8 \times 10^{5} \) | ~ 0.04 % | Étoiles massives (fusion de l'oxygène et du silicium) |
| Argon | Ar | \( 1.0 \times 10^{5} \) | ~ 0.01 % | Étoiles massives (fusion du silicium) |
| Nickel | Ni | \( 5.0 \times 10^{4} \) | ~ 0.008 % | Supernovae (effondrement de cœur, type Ia) |
| Calcium | Ca | \( 5.0 \times 10^{4} \) | ~ 0.005 % | Étoiles massives (fusion du silicium) |
| Aluminium | Al | \( 4.5 \times 10^{4} \) | ~ 0.003 % | Étoiles massives, supernovae |
| Sodium | Na | \( 2.2 \times 10^{4} \) | ~ 0.001 % | Étoiles massives, étoiles AGB |
| Tous autres éléments | — | < \( 1.0 \times 10^{4} \) | < 0.002 % | Supernovae, fusion de naines blanches, collisions d'étoiles à neutrons, processus s |
N.B.: Les valeurs d'abondance sont basées sur les données spectroscopiques du Soleil et du milieu interstellaire, constituant la référence standard en astrophysique. L'abondance est normalisée à \( 10^6 \) atomes de silicium (Si), convention courante en astronomie. L'hydrogène et l'hélium représentent à eux seuls environ 98 % de la masse baryonique ordinaire de l'Univers. La fraction de masse des éléments plus lourds que l'hélium (la "métallicité") est donc d'environ 2 % dans le voisinage solaire.
Les étoiles sont les réacteurs alchimiques de l'Univers. Dans leurs cœurs incandescents, la pression et la température sont si élevées que les noyaux atomiques fusionnent. Cette réaction, régie par l'équilibre entre la gravité et la pression de radiation, suit une hiérarchie précise.
L'hydrogène fusionne en hélium, libérant l'énergie qui fait briller les étoiles. Quand l'hydrogène du cœur s'épuise, une étoile massive (plus de 8 masses solaires) commence à fusionner l'hélium en carbone, puis le carbone en néon, et ainsi de suite, formant des couches concentriques comme un oignon. Cette chaîne de fusion s'arrête au fer \( (^{56}\text{Fe}) \), l'élément le plus stable. Le fer est le cimetière nucléaire: sa fusion ne libère plus d'énergie, elle en consomme. Le cœur de fer s'effondre alors brutalement, déclenchant une gigantesque explosion de supernova (type II).
C'est dans cette fraction de seconde et dans les vents stellaires qui suivent que sont forgés tous les éléments plus lourds que le fer. Le tableau périodique, du cobalt à l'uranium, est le fruit de ces cataclysmes stellaires. Sans les supernovae, l'Univers serait resté un lieu stérile, composé uniquement d'hydrogène, d'hélium et de quelques traces de lithium.
| Site de nucléosynthèse | Éléments principalement produits | Processus physique | Rôle dans l'évolution cosmique |
|---|---|---|---|
| Big Bang (premiers instants) | Hydrogène (¹H), Hélium (⁴He), traces de Lithium (⁷Li) | Nucléosynthèse primordiale | Fondement de toute matière baryonique, composition initiale du cosmos. |
| Étoiles de faible masse (< 8 M☉) | Hélium (⁴He), Carbone (¹²C), Azote (¹⁴N) | Fusion hydrogène et hélium, processus s (lent) lors de la phase AGB | Enrichissement du milieu interstellaire en éléments légers, essentiels à la chimie organique. |
| Étoiles massives (> 8 M☉) | Oxygène (¹⁶O), Silicium (²⁸Si), Magnésium (²⁴Mg), jusqu'au Fer (⁵⁶Fe) | Fusion hydrogène, hélium, carbone, néon, oxygène, silicium | Création des éléments constitutifs des roches et des noyaux planétaires. |
| Supernovae (effondrement de cœur) | Éléments plus lourds que le fer: Nickel (⁵⁸Ni), Cobalt (⁵⁹Co), Zinc (⁶⁴Zn), jusqu'à l'Uranium (²³⁸U) | Capture rapide de neutrons (processus r) et onde de choc explosive | Dispersion des éléments lourds dans le milieu interstellaire, essentiels pour les technologies et la radioactivité. |
| Fusion de naines blanches (type Ia) | Fer (⁵⁶Fe), Nickel (⁵⁸Ni), éléments du groupe du fer | Combustion explosive du carbone et de l'oxygène | Contribution majeure à l'abondance du fer, marqueur chimique de l'âge des populations stellaires. |
L'abondance des éléments chimiques n'est pas seulement un catalogue. C'est un outil d'archéologie stellaire. En analysant la lumière d'une étoile, son spectre, les astrophysiciens peuvent déterminer sa composition chimique. Cette signature chimique agit comme un fossile, révélant l'époque de sa naissance.
Les étoiles les plus anciennes, formées il y a plus de 10 milliards d'années, sont extrêmement pauvres en métaux (éléments plus lourds que l'hélium). Ce sont des étoiles de population II, souvent situées dans le halo galactique et les amas globulaires. À l'inverse, les jeunes étoiles, comme notre Soleil, sont riches en métaux (population I), témoignant de cycles successifs de nucléosynthèse et d'enrichissement.
Une découverte fascinante est celle des étoiles "ultra-métal-pauvres", comme SMSS J031300.36-670839.3. Découverte en 2014, elle présente une abondance en fer plus d'un million de fois inférieure à celle du Soleil, mais une quantité relativement élevée de carbone. Cela suggère que sa matière première provenait d'une première génération d'étoiles massives (population III) qui a enrichi le milieu en carbone avant d'exploser en supernova, mais sans produire beaucoup de fer. C'est une preuve directe de la diversité des processus physiques à l'œuvre dans l'Univers primitif.
Les collisions de galaxies et les fusions jouent également un rôle majeur. Lorsque deux galaxies spirales entrent en collision, comme dans le cas d'Arp 220, d'immenses nuages de gaz sont compressés, déclenchant des sursauts de formation d'étoiles massives. Ces étoiles, qui vivent rapidement et meurent en supernovae, enrichissent brutalement le milieu en éléments lourds. L'abondance chimique n'est donc pas statique: elle est le reflet dynamique de l'histoire gravitationnelle et évolutive de chaque galaxie.
L'émergence de la vie, telle que nous la connaissons, est une conséquence directe de cette longue évolution chimique. Le carbone, élément central de la chimie organique, est le produit de la fusion de l'hélium dans les étoiles (processus triple alpha). L'oxygène, que nous respirons, est le troisième élément le plus abondant dans l'Univers, forgé dans les cœurs des étoiles massives. L'azote, composant des acides aminés, est synthétisé lors des cycles CNO (carbone-azote-oxygène) dans les étoiles.
La formation des planètes rocheuses est elle-même conditionnée par l'abondance des éléments réfractaires comme le silicium, le fer, le magnésium et l'aluminium. Dans les régions de l'Univers où la métallicité est trop faible, la probabilité de former des planètes telluriques s'effondre. On peut donc tracer un lien direct, une causalité physique, entre le taux de formation des supernovae, l'enrichissement chimique du milieu interstellaire et la possibilité d'émergence de mondes habitables. La célèbre phrase de Carl Sagan (1934-1996), tirée de son livre Cosmos (1980), trouve ici son ancrage le plus profond: "Nous sommes tous des poussières d’étoiles".
L'hydrogène (environ 71 % de la masse) et l'hélium (environ 27 %). À eux deux, ils représentent environ 98 % de la matière ordinaire (baryonique) de l'Univers. Tous les autres éléments – que les astrophysiciens appellent "métaux", même le carbone et l'oxygène – ne constituent que les 2 % restants.
Parce que la nucléosynthèse primordiale n'a duré qu'environ trois minutes. L'Univers s'est refroidi et dilué trop rapidement pour que les noyaux puissent fusionner au-delà du lithium. De plus, il n'existait pas encore d'étoiles pour pousser les réactions de fusion plus loin. Pour créer du carbone, de l'oxygène ou du fer, il a fallu attendre la formation des premières étoiles massives et leurs explosions en supernovae.
Par fusion nucléaire. Dans leur cœur brûlant, la pression et la température sont si élevées que les noyaux atomiques s'assemblent. L'hydrogène fusionne d'abord en hélium, libérant l'énergie qui fait briller l'étoile. Dans les étoiles massives (plus de 8 masses solaires), ce processus se poursuit: l'hélium fusionne en carbone, le carbone en néon, puis en oxygène, silicium, et enfin en fer. Chaque étape nécessite des températures et pressions plus extrêmes.
Parce que le fer (56Fe) est l'élément le plus stable du noyau atomique. Fusionner du fer ne libère pas d'énergie – au contraire, cela en consomme. Quand une étoile massive a transformé son cœur en fer, la fusion s'arrête brutalement. Sans pression de radiation pour contrer la gravité, le cœur s'effondre en une fraction de seconde, provoquant l'explosion de la supernova. C'est dans cette explosion que sont forgés tous les éléments plus lourds que le fer (du cobalt à l'uranium).
Les étoiles les plus anciennes (population II), formées il y a plus de 10 milliards d'années, sont très pauvres en métaux (éléments plus lourds que l'hélium) car elles sont nées d'un gaz interstellaire peu enrichi par les générations stellaires précédentes. Les jeunes étoiles comme notre Soleil (population I) sont riches en métaux, témoignant de cycles successifs de nucléosynthèse et d'enrichissement. C'est un peu comme l'archéologie stellaire: la composition chimique d'une étoile est un fossile qui révèle son âge.
Ce sont des étoiles extrêmement anciennes, contenant jusqu'à un million de fois moins de fer que le Soleil. L'une d'elles, SMSS J031300.36-670839.3, découverte en 2014, a révélé une abondance relative élevée de carbone mais très peu de fer. Cela prouve que sa matière première provenait d'une toute première génération d'étoiles massives (population III) qui a enrichi le milieu en carbone avant d'exploser, mais sans produire beaucoup de fer. Ces étoiles sont des vestiges directs des premières générations stellaires de l'Univers.
L'oxygène est le troisième élément le plus abondant de l'Univers. Il est principalement forgé dans le cœur des étoiles massives, par fusion du carbone et du néon, avant d'être dispersé dans l'espace lors de leur explosion en supernova. L'oxygène que vous inspirez est donc bien le produit d'une explosion stellaire survenue il y a des milliards d'années dans une région lointaine de notre galaxie.
La vie, telle que nous la connaissons, est une conséquence directe de cette évolution chimique. Le carbone, central pour la chimie organique, est produit par fusion de l'hélium (processus triple alpha). L'azote, composant des acides aminés, est synthétisé dans les cycles CNO (carbone-azote-oxygène) des étoiles. L'oxygène est indispensable à la respiration. De plus, la formation des planètes rocheuses dépend de l'abondance des éléments réfractaires comme le silicium, le fer ou le magnésium. Dans les régions trop pauvres en métaux, la probabilité de former des mondes habitables s'effondre.
C'est une célèbre phrase de Carl Sagan qui résume une vérité physique fondamentale: tous les éléments chimiques qui composent notre corps – le carbone de nos molécules, l'oxygène de notre eau, le fer de notre sang, le calcium de nos os – ont été fabriqués dans le cœur d'étoiles massives aujourd'hui disparues, puis dispersés dans l'espace par des explosions de supernovae. Notre matière est littéralement née d'anciens soleils morts depuis des milliards d'années.
Oui, de manière majeure. Quand deux galaxies spirales entrent en collision, d'immenses nuages de gaz sont compressés, déclenchant des sursauts de formation d'étoiles massives. Ces étoiles vivent rapidement et meurent en supernovae, enrichissant brutalement le milieu interstellaire en éléments lourds. L'abondance chimique n'est donc pas statique: elle reflète l'histoire gravitationnelle et évolutive de chaque galaxie.