

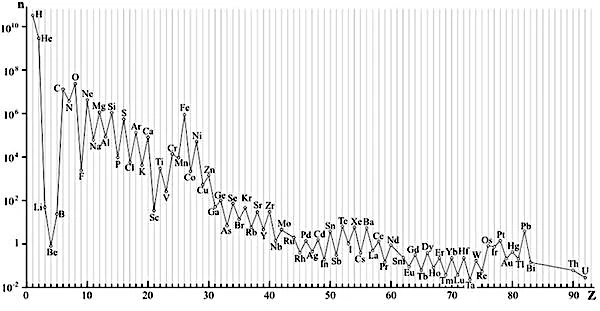
Porque esses dois elementos são os únicos produzidos em quantidades massivas durante a nucleossíntese primordial, nos três primeiros minutos após o Big Bang, há 13,8 bilhões de anos. Naquela época, o Universo em resfriamento permitiu que os primeiros prótons e nêutrons se unissem para formar cerca de 75% de hidrogênio e 25% de hélio, com apenas vestígios ínfimos de lítio e berílio. Todos os outros elementos da tabela periódica – o carbono que compõe nossos corpos, o oxigênio que respiramos, o ferro de nossas hemácias – foram forjados muito mais tarde, no coração das estrelas por meio de fusão nuclear, e então dispersos no espaço pelas violentas explosões de supernovas. A química do Universo é, portanto, uma história em dois tempos: uma composição inicial herdada do Big Bang, seguida por um enriquecimento progressivo por sucessivas gerações estelares, fazendo de nós, literalmente, "poeira das estrelas".
Nos primeiros instantes após o Big Bang, há cerca de 13,8 bilhões de anos, o Universo era uma sopa de quarks e glúons de densidade e temperatura inimagináveis. Ao esquentar, os primeiros prótons e nêutrons se juntaram. Durante os três primeiros minutos, o cosmos foi palco de uma nucleossíntese primordial fulgurante. O resultado dessa alquimia original é de uma simplicidade absoluta: cerca de 75% de hidrogênio (¹H) e 25% de hélio (⁴He), com traços mínimos de lítio e berílio.
Essa herança inicial, essa abundância primordial, é a partitura básica sobre a qual toda a história cósmica será escrita. Nenhum elemento mais pesado que o lítio pôde surgir dessa época. Para criar carbono, oxigênio, ferro e todos os átomos que hoje constituem os planetas, os oceanos e nossos próprios corpos, foi necessário esperar o nascimento, a vida e a morte violenta das primeiras estrelas. Margaret Burbidge (1919-2020), astrofísica pioneira, marcou profundamente o estudo da formação dos elementos químicos dentro das estrelas e da estrutura das galáxias. Graças às suas pesquisas, agora sabemos que somos, no sentido literal, compostos de "poeira de estrelas".
| Elemento | Símbolo | Abundância relativa (átomos) (normalizada a 10⁶ átomos de Si) | Relação de massa (fração em %) | Principais locais de produção |
|---|---|---|---|---|
| Hidrogênio | H | \( 4.0 \times 10^{10} \) | ~ 71 % | Big Bang (nucleossíntese primordial) |
| Hélio | He | \( 3.0 \times 10^{9} \) | ~ 27 % | Big Bang, fusão estelar |
| Oxigênio | O | \( 2.2 \times 10^{7} \) | ~ 0.9 % | Estrelas massivas (fusão de C, Ne, O), supernovas |
| Carbono | C | \( 1.0 \times 10^{7} \) | ~ 0.3 % | Estrelas de baixa massa (processo triplo alfa), estrelas massivas |
| Neônio | Ne | \( 1.8 \times 10^{6} \) | ~ 0.1 % | Estrelas massivas (fusão do carbono) |
| Nitrogênio | N | \( 6.2 \times 10^{5} \) | ~ 0.09 % | Estrelas de baixa massa (processo CNO), estrelas massivas |
| Silício | Si | \( 1.0 \times 10^{6} \) | ~ 0.07 % | Estrelas massivas (fusão do oxigênio, fusão do silício) |
| Magnésio | Mg | \( 1.0 \times 10^{6} \) | ~ 0.06 % | Estrelas massivas (fusão do neônio e do carbono) |
| Ferro | Fe | \( 8.3 \times 10^{5} \) | ~ 0.12 % | Supernovas (colapso do núcleo), supernovas do tipo Ia |
| Enxofre | S | \( 4.8 \times 10^{5} \) | ~ 0.04 % | Estrelas massivas (fusão do oxigênio e do silício) |
| Argônio | Ar | \( 1.0 \times 10^{5} \) | ~ 0.01 % | Estrelas massivas (fusão do silício) |
| Níquel | Ni | \( 5.0 \times 10^{4} \) | ~ 0.008 % | Supernovas (colapso do núcleo, tipo Ia) |
| Cálcio | Ca | \( 5.0 \times 10^{4} \) | ~ 0.005 % | Estrelas massivas (fusão do silício) |
| Alumínio | Al | \( 4.5 \times 10^{4} \) | ~ 0.003 % | Estrelas massivas, supernovas |
| Sódio | Na | \( 2.2 \times 10^{4} \) | ~ 0.001 % | Estrelas massivas, estrelas AGB |
| Todos os outros elementos | — | < \( 1.0 \times 10^{4} \) | < 0.002 % | Supernovas, fusão de anãs brancas, colisões de estrelas de nêutrons, processo s |
N.B.: Os valores de abundância são baseados em dados espectroscópicos do Sol e do meio interestelar, que constituem a referência padrão em astrofísica. A abundância é normalizada a \( 10^6 \) átomos de silício (Si), convenção comum em astronomia. O hidrogênio e o hélio representam sozinhos cerca de 98% da massa bariônica ordinária do Universo. A fração de massa dos elementos mais pesados que o hélio (a "metalicidade") é, portanto, de cerca de 2% na vizinhança solar.
As estrelas são os reatores alquímicos do Universo. Em seus núcleos incandescentes, a pressão e a temperatura são tão elevadas que os núcleos atômicos se fundem. Essa reação, regida pelo equilíbrio entre a gravidade e a pressão de radiação, segue uma hierarquia precisa.
O hidrogênio se funde em hélio, liberando a energia que faz as estrelas brilharem. Quando o hidrogênio do núcleo se esgota, uma estrela massiva (mais de 8 massas solares) começa a fundir o hélio em carbono, depois o carbono em neônio, e assim por diante, formando camadas concêntricas como uma cebola. Essa cadeia de fusão para no ferro \( (^{56}\text{Fe}) \), o elemento mais estável. O ferro é o cemitério nuclear: sua fusão não libera mais energia, consome-a. O núcleo de ferro então colapsa abruptamente, desencadeando uma gigantesca explosão de supernova (tipo II).
É nessa fração de segundo e nos ventos estelares que se seguem que todos os elementos mais pesados que o ferro são forjados. A tabela periódica, do cobalto ao urânio, é o fruto desses cataclismos estelares. Sem as supernovas, o Universo teria permanecido um lugar estéril, composto apenas de hidrogênio, hélio e alguns traços de lítio.
| Local de nucleossíntese | Elementos produzidos principalmente | Processo físico | Papel na evolução cósmica |
|---|---|---|---|
| Big Bang (primeiros instantes) | Hidrogênio (¹H), Hélio (⁴He), traços de Lítio (⁷Li) | Nucleossíntese primordial | Fundamento de toda a matéria bariônica, composição inicial do cosmos. |
| Estrelas de baixa massa (< 8 M☉) | Hélio (⁴He), Carbono (¹²C), Nitrogênio (¹⁴N) | Fusão de hidrogênio e hélio, processo s (lento) durante a fase AGB | Enriquecimento do meio interestelar em elementos leves, essenciais para a química orgânica. |
| Estrelas massivas (> 8 M☉) | Oxigênio (¹⁶O), Silício (²⁸Si), Magnésio (²⁴Mg), até Ferro (⁵⁶Fe) | Fusão de hidrogênio, hélio, carbono, neônio, oxigênio, silício | Criação dos elementos constitutivos das rochas e dos núcleos planetários. |
| Supernovas (colapso do núcleo) | Elementos mais pesados que o ferro: Níquel (⁵⁸Ni), Cobalto (⁵⁹Co), Zinco (⁶⁴Zn), até Urânio (²³⁸U) | Captura rápida de nêutrons (processo r) e onda de choque explosiva | Dispersão de elementos pesados no meio interestelar, essenciais para tecnologias e radioatividade. |
| Fusão de anãs brancas (tipo Ia) | Ferro (⁵⁶Fe), Níquel (⁵⁸Ni), elementos do grupo do ferro | Combustão explosiva do carbono e do oxigênio | Contribuição majoritária para a abundância do ferro, marcador químico da idade das populações estelares. |
A abundância dos elementos químicos não é apenas um catálogo. É uma ferramenta de arqueologia estelar. Ao analisar a luz de uma estrela, seu espectro, os astrofísicos podem determinar sua composição química. Essa assinatura química age como um fóssil, revelando a época de seu nascimento.
As estrelas mais antigas, formadas há mais de 10 bilhões de anos, são extremamente pobres em metais (elementos mais pesados que o hélio). São estrelas da População II, frequentemente encontradas no halo galáctico e nos aglomerados globulares. Em contraste, as estrelas jovens, como o nosso Sol, são ricas em metais (População I), testificando ciclos sucessivos de nucleossíntese e enriquecimento.
Uma descoberta fascinante é a das estrelas "ultra pobres em metais", como SMSS J031300.36-670839.3. Descoberta em 2014, ela apresenta uma abundância de ferro mais de um milhão de vezes inferior à do Sol, mas uma quantidade relativamente elevada de carbono. Isso sugere que sua matéria-prima proveio de uma primeira geração de estrelas massivas (População III) que enriqueceu o meio com carbono antes de explodir como supernovas, mas sem produzir muito ferro. É uma prova direta da diversidade dos processos físicos em ação no Universo primitivo.
As colisões de galáxias e as fusões também desempenham um papel importante. Quando duas galáxias espirais colidem, como no caso de Arp 220, imensas nuvens de gás são comprimidas, desencadeando surtos de formação de estrelas massivas. Essas estrelas, que vivem rapidamente e morrem como supernovas, enriquecem bruscamente o meio com elementos pesados. A abundância química não é, portanto, estática: é o reflexo dinâmico da história gravitacional e evolutiva de cada galáxia.
A emergência da vida, como a conhecemos, é uma consequência direta dessa longa evolução química. O carbono, elemento central da química orgânica, é o produto da fusão do hélio nas estrelas (processo triplo alfa). O oxigênio, que respiramos, é o terceiro elemento mais abundante no Universo, forjado nos núcleos das estrelas massivas. O nitrogênio, componente dos aminoácidos, é sintetizado durante os ciclos CNO (carbono-nitrogênio-oxigênio) nas estrelas.
A formação de planetas rochosos é condicionada pela abundância de elementos refratários como o silício, o ferro, o magnésio e o alumínio. Nas regiões do Universo onde a metalicidade é muito baixa, a probabilidade de formar planetas telúricos desaba. Podemos, portanto, traçar uma ligação direta, uma causalidade física, entre a taxa de formação de supernovas, o enriquecimento químico do meio interestelar e a possibilidade de emergência de mundos habitáveis. A famosa frase de Carl Sagan (1934-1996), retirada de seu livro Cosmos (1980), encontra aqui seu ancoradouro mais profundo: "Somos todos feitos de poeira de estrelas".
Hidrogênio (cerca de 71% da massa) e hélio (cerca de 27%). Juntos, representam aproximadamente 98% de toda a matéria ordinária (bariônica) do Universo. Todos os outros elementos – que os astrofísicos chamam de "metais", mesmo o carbono e o oxigênio – constituem apenas os 2% restantes.
Porque a nucleossíntese primordial durou apenas cerca de três minutos. O Universo esfriou e se diluiu rápido demais para que os núcleos pudessem fundir-se além do lítio. Além disso, as estrelas ainda não existiam para impulsionar as reações de fusão. Para criar carbono, oxigênio ou ferro, foi necessária a formação das primeiras estrelas massivas e suas explosões como supernovas.
Por meio da fusão nuclear. Em seus núcleos ardentes, a pressão e a temperatura são tão altas que os núcleos atômicos se fundem. O hidrogênio primeiro se funde em hélio, liberando a energia que faz a estrela brilhar. Em estrelas massivas (mais de 8 massas solares), esse processo continua: o hélio se funde em carbono, o carbono em neônio, depois em oxigênio, silício e finalmente em ferro. Cada etapa exige temperaturas e pressões cada vez mais extremas.
Porque o ferro (⁵⁶Fe) é o núcleo atômico mais estável. Fundir ferro não libera energia – ao contrário, consome energia. Quando uma estrela massiva transforma seu núcleo em ferro, a fusão para abruptamente. Sem a pressão de radiação para contrapor a gravidade, o núcleo colapsa em uma fração de segundo, desencadeando a explosão da supernova. É nessa explosão que são forjados todos os elementos mais pesados que o ferro (do cobalto ao urânio).
As estrelas mais antigas (População II), formadas há mais de 10 bilhões de anos, são muito pobres em metais (elementos mais pesados que o hélio) porque nasceram de gás interestelar pouco enriquecido por gerações estelares anteriores. Estrelas jovens como o nosso Sol (População I) são ricas em metais, testemunhando sucessivos ciclos de nucleossíntese e enriquecimento. É uma forma de arqueologia estelar: a composição química de uma estrela é um fóssil que revela sua idade.
São estrelas extremamente antigas, contendo até um milhão de vezes menos ferro que o Sol. Uma delas, SMSS J031300.36-670839.3, descoberta em 2014, revelou uma abundância relativamente alta de carbono mas muito pouco ferro. Isso prova que seu material de origem veio de uma primeira geração de estrelas massivas (População III) que enriqueceu o meio com carbono antes de explodir, mas sem produzir muito ferro. Essas estrelas são vestígios diretos das primeiras gerações estelares do Universo.
O oxigênio é o terceiro elemento mais abundante do Universo. Ele é forjado principalmente no núcleo de estrelas massivas, por meio da fusão do carbono e do neônio, antes de ser disperso no espaço durante suas explosões como supernovas. O oxigênio que você inspira é, portanto, verdadeiramente produto de uma explosão estelar ocorrida há bilhões de anos em uma região distante da nossa galáxia.
A vida como a conhecemos é uma consequência direta dessa evolução química. O carbono, central para a química orgânica, é produzido pela fusão do hélio (processo triplo-alfa). O nitrogênio, componente dos aminoácidos, é sintetizado nos ciclos CNO (carbono-nitrogênio-oxigênio) das estrelas. O oxigênio é essencial para a respiração. Além disso, a formação de planetas rochosos depende da abundância de elementos refratários como silício, ferro e magnésio. Em regiões muito pobres em metais, a probabilidade de formar mundos habitáveis desmorona.
É uma famosa frase de Carl Sagan que resume uma verdade física fundamental: todos os elementos químicos que compõem nosso corpo – o carbono de nossas moléculas, o oxigênio de nossa água, o ferro de nosso sangue, o cálcio de nossos ossos – foram fabricados no núcleo de estrelas massivas já desaparecidas, e então dispersos no espaço por explosões de supernovas. Nossa matéria nasce literalmente de antigos sóis que morreram há bilhões de anos.
Sim, de maneira significativa. Quando duas galáxias espirais colidem, imensas nuvens de gás são comprimidas, desencadeando surtos de formação de estrelas massivas. Essas estrelas vivem rápido e morrem como supernovas, enriquecendo abruptamente o meio interestelar com elementos pesados. A abundância química não é, portanto, estática: ela reflete a história gravitacional e evolutiva de cada galáxia.