

Na natureza, toda a matéria está concentrada na energia de massa dos núcleos, que são 100.000 vezes menores que o átomo, mas milhares de vezes mais pesados que todos os seus elétrons.
Na matéria, muitos núcleos atômicos são estáveis e seu estado permanece indefinidamente igual. Um isótopo é estável quando tem um número harmonioso de prótons e nêutrons. Por outro lado, muitos núcleos são instáveis porque possuem muitos prótons ou nêutrons, ou ambos. Os físicos identificaram pouco menos de 300 isótopos estáveis e cerca de 3.000 instáveis. Se os núcleos são instáveis, é devido à barreira de Coulomb, que estabelece uma competição entre a força de repulsão eletrostática entre prótons e a força nuclear atraente entre nêutrons e prótons. Por isso, os núcleos devem incorporar cada vez mais nêutrons à medida que crescem.
Todos os núcleos da matéria buscam uma estabilidade energética frugal. Assim, para retornar a um estado estável, eles devem se transformar expulsando energia na forma de massa ou radiação (E=mc²). Isso é chamado de radioatividade.
Esse fenômeno de radioatividade natural está presente em toda a matéria, tanto em minerais quanto em nossos alimentos (a Comunidade Europeia estabeleceu limites de radioatividade nos alimentos) e até mesmo em nossos corpos (devido à presença de carbono-14 e potássio-40).
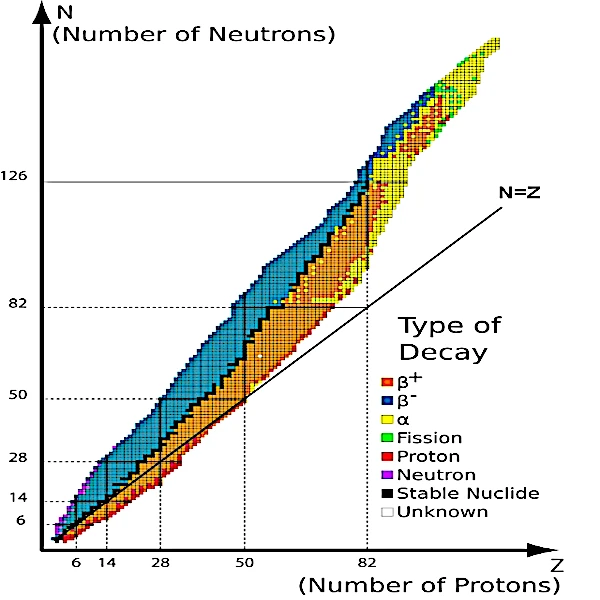
• Quando todos os isótopos conhecidos são representados em um gráfico (imagem acima) por seu número de prótons (Z) e seu número de nêutrons (N), observa-se que todos os isótopos estáveis (pontos pretos) estão agrupados ao redor de uma linha. Esta linha está no fundo de um vale chamado "vale da estabilidade".
Os núcleos instáveis estão distribuídos nos flancos do vale, de ambos os lados dessa linha preta que representa o rio de matéria estável fluindo no fundo do vale. Quanto mais instáveis são os núcleos, mais altos estão no vale. Assim, neste vale, o caminho mais curto para alcançar a estabilidade é descer até o fundo do vale.
• Os nucleídeos no flanco esquerdo do vale (em azul na imagem), com excesso de nêutrons em comparação com seu número de prótons, encontram estabilidade através de uma cascata de desintegrações β- com emissão de elétrons e neutrinos, que lhes permite descer gradualmente pelas encostas do vale.
• Os nucleídeos no flanco direito do vale (em laranja), com excesso de prótons, encontram estabilidade através de uma cascata de desintegrações β+ com emissão de pósitrons e neutrinos.
• Os nucleídeos na pequena crista esquerda do vale (em roxo) na borda exterior da zona azul, encontram estabilidade através da emissão de nêutrons; o núcleo mantém o mesmo número atômico (Z) mas sua massa atômica diminui.
• Os nucleídeos localizados na pequena crista direita do vale (em vermelho) na borda exterior da zona laranja, encontram estabilidade através da emissão de prótons; o número atômico (Z) e a massa atômica do núcleo diminuem.
• No caso dos núcleos muito pesados, a fissão intervém. Os nucleídeos, além da linha dos isótopos estáveis (em verde claro), encontram estabilidade através da divisão do núcleo em dois núcleos mais leves com emissão de um ou mais nêutrons.
• Os nucleídeos de alta massa atômica (em amarelo) sofrem uma desintegração α frequentemente acompanhada pela emissão de fotons de alta energia ou raios gama. Se a inclinação for muito alta, as desintegrações β se intercalam entre as desintegrações α. Uma cascata de desintegrações radioativas é necessária para alcançar o fundo do vale.
• Finalmente, os núcleos particularmente estáveis possuem um certo número de nucleons (2, 8, 20, 28, 50, 82 e 126) que correspondem ao modelo em camadas do núcleo atômico (níveis de energia quantificados baseados no princípio de exclusão de Pauli). Esses números chamados mágicos estão marcados ao longo dos degraus da curva preta. Os núcleos que têm tanto um número mágico de prótons quanto de nêutrons e um número de prótons igual ao número de nêutrons são chamados de duplamente mágicos porque são muito estáveis.
Esse é o caso do chumbo-208, que é composto por 82 prótons e 126 nêutrons, e do cálcio-48, que é composto por 20 prótons e 28 nêutrons.
• As descontinuidades na curva preta em nêutrons (19, 21, 35, 39, 45, 84, 115 e 123) e em prótons (43 e 61) correspondem aos casos em que não há núcleos estáveis com essas quantidades de nucleons.
O vale da estabilidade contém cerca de 3.000 nucleídeos observados, estáveis, instáveis e muito instáveis. Mas não conhecemos os limites de estabilidade (linhas de gotejamento) dos nucleídeos. Para os prótons (número máximo de prótons), é relativamente conhecido através da tabela de Mendeleev. Para os nêutrons (número máximo de nêutrons), os limites de estabilidade são conhecidos apenas para os primeiros elementos, do hidrogênio ao oxigênio-15. Por exemplo, para Z=8, o número máximo de nêutrons é 16, fazendo do oxigênio-24 o isótopo mais pesado possível do oxigênio. O alcance completo do vale da estabilidade continua desconhecido e parece que o que resta para descobrir é enorme.
N.B.:
O núcleo do átomo é composto por prótons e nêutrons. Átomos do mesmo elemento químico têm o mesmo número de prótons, mas podem ter um número diferente de nêutrons; esses são os isótopos. Átomos estáveis não sofrem desintegração radioativa.