

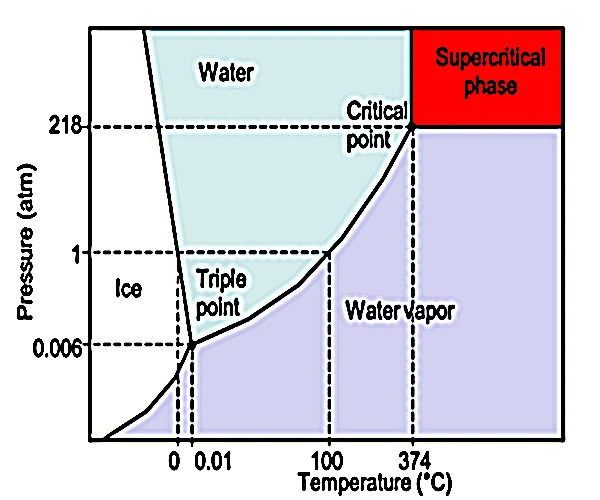
O estado supercrítico da água, atingido a uma temperatura de 374 °C e uma pressão de 22,06 MPa (≈217,8 atm), é um domínio termodinâmico no qual a água já não se distingue entre líquido e gás. Nesta zona, ela possui tanto a densidade de um líquido como a difusividade de um gás. Este comportamento híbrido abre caminho para propriedades físicas e químicas únicas, tornando-a muito reativa, excelente para dissolver substâncias orgânicas e inorgânicas, e amplamente utilizada em geoquímica, processos industriais e até na exploração de condições pré-bióticas.
Ao contrário da água líquida ou vapor, a água supercrítica apresenta flutuações significativas de densidade em pequena escala, o que modifica as constantes dielétricas, a solvatação iônica e os mecanismos de transporte térmico. Ela pode dissolver sais como um líquido, mas comportar-se como um gás para espécies não polares. Sua condutividade térmica é elevada, sua viscosidade baixa e sua tensão superficial é nula. Estas características fazem dela um excelente fluido de trabalho ou solvente verde em processos de química sustentável.
O estado supercrítico da água só pode existir a pressões superiores a 217 atm e temperaturas além de 374 °C. Estas condições são naturalmente reunidas em certos ambientes geotérmicos profundos, nomeadamente na crosta oceânica e nas proximidades das câmaras magmáticas. Pode ser encontrada nas seguintes áreas:
Estes ambientes extremos são de grande interesse tanto para a pesquisa fundamental (origem da vida, extremófilos, mineralização) como para as tecnologias emergentes de geoenergia.
A água supercrítica é encontrada em diversos domínios:
O estado supercrítico da água pode ter desempenhado um papel na origem da vida na Terra. Em ambientes hidrotermais profundos, a água supercrítica pode ter favorecido reações orgânicas complexas, precursoras do aparecimento das primeiras moléculas biológicas. Além disso, as propriedades excepcionais de solvatação e catálise podem ter servido de suporte ao desenvolvimento de químicas pré-bióticas na superfície ou na crosta terrestre.
| Propriedade | Líquido | Vapor | Supercrítico |
|---|---|---|---|
| Densidade (kg/m³) | 1000 | 0.6 | 200-500 |
| Viscosidade (μPa·s) | 890 | 13 | 100-300 |
| Constante dielétrica | ≈80 | ≈1.0 | ≈10-20 |
| Solubilidade de sais | Forte | Nula | Média a forte (variável) |
| Tensão superficial | 72 mN/m | Nula | Nula |
Fonte: NIST Chemistry WebBook, ScienceDirect - Supercritical water oxidation.