

In der Natur ist die gesamte Materie in der Massenenergie von Kernen konzentriert, die 100.000-mal kleiner als das Atom, aber tausendmal schwerer als alle ihre Elektronen sind.
In der Materie sind viele Atomkerne stabil und ihr Zustand bleibt auf unbestimmte Zeit derselbe. Ein Isotop ist stabil, wenn es eine harmonische Anzahl von Protonen und Neutronen aufweist. Andererseits sind viele Kerne instabil, weil sie zu viele Protonen oder Neutronen oder zu viel von beidem haben. Physiker haben knapp 300 stabile und fast 3.000 instabile Isotope identifiziert. Wenn die Kerne instabil sind, liegt das an der Coulomb-Barriere, die einen Wettbewerb zwischen der elektrostatischen Abstoßungskraft zwischen den Protonen und der anziehenden Kernkraft zwischen den Neutronen und den Protonen herstellt. Deshalb müssen die Kerne im Laufe ihres Wachstums immer mehr Neutronen integrieren.
Alle Materiekerne streben nach sparsamer energetischer Stabilität. Um in einen stabilen Zustand zurückzukehren, müssen sie sich umwandeln, indem sie Energie in Form von Masse oder Strahlung ausstoßen (E=mc2). Dies nennt man Radioaktivität.
Dieses Phänomen der natürlichen Radioaktivität ist überall in der Materie am Werk, sowohl in Mineralien als auch in unserer Nahrung (die Europäische Gemeinschaft hat Radioaktivitätsdosen festgelegt, die in Nahrungsmitteln nicht überschritten werden dürfen) und sogar in unserem Körper (aufgrund des Vorhandenseins von Kohlenstoff 14 und Kalium 40).
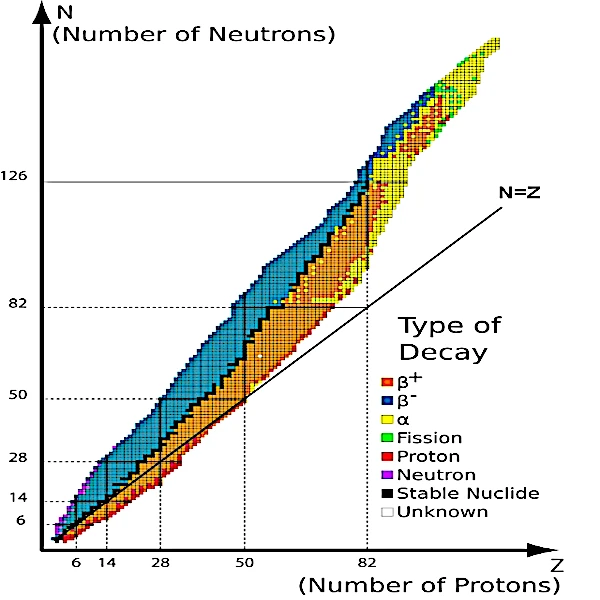
• Wenn wir alle bekannten Isotope in einem Diagramm (Bild oben) anhand ihrer Anzahl an Protonen (Z) und ihrer Anzahl an Neutronen (N) darstellen, sehen wir, dass alle stabilen Isotope (schwarze Punkte) um eine Linie gruppiert sind. Diese Linie liegt am Grund eines Tals, das „Stabilitätstal“ genannt wird.
Die instabilen Kerne sind an den Seiten des Tals auf beiden Seiten dieser schwarzen Linie verteilt, die den Fluss aus stabilem Material darstellt, der zum Talboden fließt. Je instabiler die Kerne sind, desto höher liegen sie im Tal. In diesem Tal ist der kürzeste Weg, Stabilität zu erreichen, der Abstieg zum Talgrund.
• Die Nuklide auf der linken Seite des Tals (in Blau im Bild), die im Vergleich zu ihrer Protonenzahl einen Überschuss an Neutronen aufweisen, gewinnen durch eine Kaskade von β-Zerfällen mit Emission von Elektronen und Neutrinos wieder an Stabilität, wodurch sie allmählich die Hänge des Tals hinabsteigen können.
• Die Nuklide auf der rechten Seite des Tals (in Orange) mit einem Überschuss an Protonen gewinnen durch eine Kaskade von β+-Zerfällen mit Emission von Positronen und Neutrinos wieder an Stabilität.
• Die Nuklide auf dem kleinen linken Kamm des Tals (in Lila) an der peripheren Grenze der blauen Zone gewinnen durch Neutronenemission wieder an Stabilität, der Kern behält die gleiche Ordnungszahl (Z), aber seine Atommasse nimmt ab.
• Die Nuklide, die sich auf dem schmalen rechten Talkamm (in Rot) an der peripheren Grenze der orangefarbenen Zone befinden, gewinnen durch die Emission von Protonen wieder an Stabilität, die Ordnungszahl (Z) und die Atommasse des Kerns nehmen ab.
• Auf der Seite sehr schwerer Kerne kommt es zur Spaltung. Die Nuklide jenseits der Linie stabiler Isotope (in Hellgrün) erlangen ihre Stabilität durch die Teilung des Kerns in zwei leichtere Kerne unter Emission eines oder mehrerer Neutronen zurück.
• Nuklide mit hoher Atommasse (gelb) durchlaufen einen α-Zerfall, der häufig mit der Emission hochenergetischer Photonen oder Gammastrahlen einhergeht. Wenn die Steigung zu hoch ist, werden β-Zerfälle zwischen den α-Zerfällen eingefügt. Um den Talboden zu erreichen, ist eine Kaskade radioaktiven Zerfalls notwendig.
• Schließlich verfügen besonders stabile Kerne über eine bestimmte Anzahl von Nukleonen (2, 8, 20, 28, 50, 82 und 126), die dem Schichtenmodell des Atomkerns (quantifizierte Energieniveaus nach dem Pauli-Ausschlussprinzip) entsprechen. Diese sogenannten magischen Zahlen befinden sich entlang der Stufen der schwarzen Kurve. Kerne, die sowohl eine magische Anzahl an Protonen und Neutronen als auch eine Anzahl an Protonen haben, die der Anzahl an Neutronen entspricht, werden als doppelt magisch bezeichnet, da sie sehr stabil sind.
Dies ist der Fall bei Blei 208, das aus 82 Protonen und 126 Neutronen besteht, und bei Kalzium 48, das aus 20 Protonen und 28 Neutronen besteht.
• Die Diskontinuitäten der schwarzen Kurve bei Neutronen (19, 21, 35, 39, 45, 84, 115 und 123) und bei Protonen (43 und 61) entsprechen Fällen, in denen es bei diesen Nukleonenmengen keinen stabilen Kern gibt.
Das Stabilitätstal enthält etwa 3000 beobachtete Nuklide, stabil, instabil und sehr instabil. Aber wir kennen die Stabilitätsgrenzen (Tropflinien) von Nukliden nicht. Für Protonen (maximale Protonenzahl) ist es durch die Mendelejew-Tabelle relativ bekannt. Für Neutronen (maximale Neutronenzahl) sind Stabilitätsgrenzen nur für die ersten paar Elemente bekannt, von Wasserstoff bis Sauerstoff 15. Beispielsweise beträgt für Z=8 die maximale Neutronenzahl 16, was Sauerstoff 24 als schwerstmögliches Sauerstoffisotop ergibt. Das volle Ausmaß des Tals der Stabilität ist noch unbekannt, und es scheint, dass es noch enorm viel zu entdecken gibt.
Hinweis: Der Atomkern besteht aus Protonen und Neutronen. Atome desselben chemischen Elements haben die gleiche Anzahl an Protonen, können aber eine unterschiedliche Anzahl an Neutronen haben, das sind Isotope. Stabile Atome unterliegen keinem radioaktiven Zerfall.