


Bien avant d'assurer la réplication, la variation puis la sélection, la vie avait besoin d'une bulle protectrice, un contenant minimum, résistant, facile à réaliser, pouvant apparaitre spontanément dans l'environnement de l'époque. Ceci se passe longtemps avant l'émergence de la cellule qui est la brique de base extrêmement complexe du vivant qui apparaitra bien plus tard entre 3,5 à 4 milliards d'années.
Les premières bulles organiques simples, se seraient formées relativement tôt dans l'histoire de la Terre, dans une période appelée l'Hadéen (entre 4,6 et 4 milliards d'années).
L'apparition des proto-membranes cellulaires résulte à la fois de processus électrostatiques et de sélection naturelle, où seules les structures les plus stables et les plus fonctionnelles ont perduré au fil du temps. Ces deux mécanismes interagissent de manière naturelle (auto-assemblage) pour favoriser l'émergence et la stabilité des premières structures. La formation des premiers assemblages moléculaires et la construction de structures biologiques comme les proto-membranes cellulaires ont pris énormément de temps en raison de la nature aléatoire des mécanismes en jeu.
Les environnements primitifs de la Terre, il y a environ 4,6 milliards d'années, étaient caractérisés par une atmosphère réduite, une activité volcanique intense, et la présence de sources hydrothermales. Ces environnements fournissaient une variété d'éléments et de composés chimiques pouvant aboutir à la formation de structures simples à base de carbone, d'hydrogène et d'oxygène (CHO).
La théorie des fumeurs blancs est une des nombreuses hypothèses sur l'origine de la vie. Il est plausible que la vie soit apparue dans les profondeurs des océans, dans des conditions qui sont encore présentes aujourd'hui. La vie pourrait avoir émergé dans des cheminées hydrothermales sous-marines, où l'eau chaude et minéralisée réagit avec des roches riches en métaux. Ces environnements aqueux pourraient avoir sélectionné des réactions chimiques favorables à la formation de molécules organiques complexes.
La formation des premiers contenants représente une étape cruciale vers l'émergence de la vie.
Cette fabrication englobe des aspects chimiques, physiques et géologiques qui interagissent pour aboutir à des structures capables de résister plus ou moins longtemps aux turbulences de l'environnement, en fonction de la température, de la taille et de la forme des molécules lipidiques.
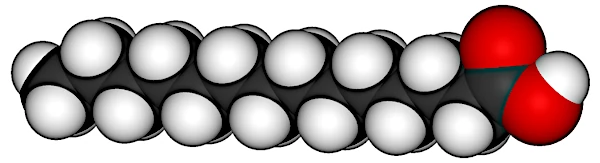
L'une des hypothèses les plus acceptées pour la formation de contenants proto-cellulaires repose sur la chimie des lipides. Les acides gras sont de bons candidats pour former des bulles à partir de sources carbonées simples comme le monoxyde de carbone et le dihydrogène à proximité des sources hydrothermales.
Les acides gras ont la propriété unique de s'auto-assembler en structures organisées lorsqu'ils sont placés dans un environnement aqueux, en raison de leur nature amphiphile (possédant une tête hydrophile et une queue hydrophobe). Ce processus d'auto-assemblage est au cœur de la formation des membranes primitives et de structures comme des micelles ou des vésicules, capables de capturer d'autres molécules et de former des compartiments fermés.
Cette dualité de nature rend les acides gras particulièrement aptes à s'organiser dans des environnements aqueux, car leurs différentes parties interagissent différemment avec l'eau.
Dans une solution aqueuse, à faible concentration, les acides gras peuvent former, grâce aux forces électromagnétiques entre les atomes, des pelotes appelées micelles, où les queues hydrophobes se regroupent au centre de la structure sphérique, tandis que les têtes hydrophiles sont orientées vers l’extérieur en contact avec l’eau.
À des concentrations plus élevées, les acides gras peuvent former des bicouches lipidiques, où les queues hydrophobes se font face et les têtes hydrophiles sont en contact avec l’eau des deux côtés. Ces bicouches flexibles, agitées par les fluctuations aléatoires de l'eau dans laquelle elles baignent, finissent par amorcer la fermeture sur elles-mêmes. Elles forment alors des vésicules (protocellules) sphériques et dynamiques relativement stables dans le temps, avec un intérieur aqueux, créant ainsi un compartiment clos.
Le processus d'auto-assemblage et d'encapsulation est amplifié par les conditions environnementales des sources hydrothermales. Dans cet environnement remuant où la température et le potentiel hydrogène (pH) fluctuent, la concentration des acides gras dans l’eau favorise la formation de vésicules. Les vésicules se forment, se déforment, se divisent et se reforment, capturant aléatoirement des molécules organiques au cours de ce cycle dynamique.
Pour que les acides gras forment des structures comme des micelles ou des vésicules, une concentration critique d'acides gras doit être atteinte. Au-delà de cette concentration, l'auto-assemblage devient spontané, et des molécules externes peuvent être capturées durant ce processus.
La capacité des vésicules d'acides gras à encapsuler des molécules est essentielle pour l'origine de la vie, car elle permet l'isolement de processus biochimiques futurs dans un environnement contrôlé.
Lorsque ces structures se forment, il est possible que des molécules organiques (comme des acides aminés, des sucres ou d'autres petites molécules) soient piégées à l'intérieur des vésicules en formation. Cette encapsulation peut se produire à un moment où la membrane se referme autour de ces molécules.
Même si la durée de vie d'une vésicule peut être limitée à quelques heures ou jours, cela est suffisant pour permettre des interactions chimiques et des réactions biochimiques. Pendant ce temps, une vésicule peut jouer un rôle crucial dans le confinement de réactions biochimiques importantes, ce qui pourrait conduire à des processus d'auto-renouvellement ou d'auto-organisation. Cela va ouvrir la voie à des réactions biochimiques fondamentales pour l'émergence de systèmes vivants plus complexes.
La vie sur Terre est supposée avoir émergé dans des environnements aqueux, comme les sources hydrothermales sous-marines. Dans ces environnements riches, les molécules pouvaient interagir et s’auto-assembler. Des structures comme des vésicules lipidiques (protocellules) ont pu se former naturellement pour enclore et protéger les premières réactions biochimiques.
Les forces électromagnétiques entre les atomes et les molécules (Van der Waals, forces coulombiennes, liaisons hydrogène) sont les moteurs fondamentaux de l'auto-assemblage naturel des acides gras en structures fermées comme les vésicules et les micelles.
Les proto-vésicules lipidiques ont permis d'enclore et de protéger les premières réactions biochimiques, préparant le terrain pour l'émergence de la vie.
N.B.:
L'abiogenèse est le processus par lequel la vie a émergé à partir de matière non vivante sur la Terre primitive. La Terre, il y a environ 4,5 milliards d'années, était une planète chaude et riche en composés chimiques, comprenant l'eau, le dioxyde de carbone, l'ammoniac, le méthane et d'autres gaz.