

El nitrógeno es indispensable para formar proteínas y ADN, pero la mayoría de los seres vivos no pueden utilizarlo en su forma gaseosa, aunque sea abundante en la atmósfera. El ciclo del nitrógeno transforma continuamente este elemento en formas aprovechables gracias a la acción de bacterias, plantas, animales y procesos naturales. Sin estas conversiones, los suelos perderían fertilidad, los océanos su productividad y los ecosistemas colapsarían. Este ciclo invisible pero fundamental mantiene el equilibrio biológico del planeta.
La atmósfera terrestre contiene casi un 78% de dinitrógeno (\(N_2\)) en volumen o un 75% en masa. Sin embargo, este enorme recurso potencial para la vida es inaccesible para la gran mayoría de los seres vivos. Ningún animal, humano o planta puede transformarlo en nutrientes.
La razón radica en la excepcional robustez del triple enlace químico entre los dos átomos de nitrógeno (N≡N). Se requiere una energía considerable para romper este enlace.
Existen dos vías: el rayo y sus 30,000 °C, o la elegancia química de las bacterias y su enzima nitrogenasa, capaz de reducir \(N_2\) a \(NH_3\) (dinitrógeno → amoníaco). Sin esta ruptura previa, no habría proteínas, ni ADN, ni músculos, ni neuronas, ni sangre: no habría vida.
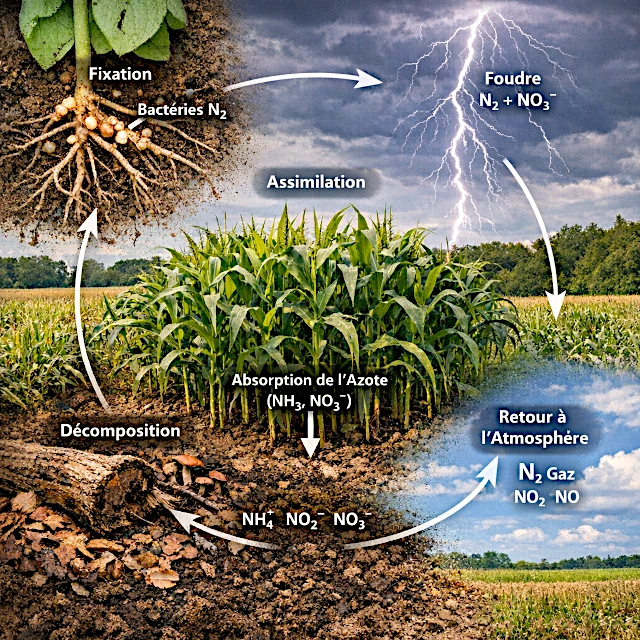
El ciclo del nitrógeno es una cascada de transformaciones que convierte un gas inerte en nutrientes asimilables, luego lo devuelve a la atmósfera.
N.B.: Antoine Lavoisier (1743-1794) propuso el término "nitrógeno" (del griego "a-zôê", sin vida). Paradójicamente, este elemento inerte en forma gaseosa resulta indispensable para toda célula viva una vez fijado.
| Proceso | Transformación química | Bacterias + Hongos | Condiciones requeridas | Rol ecológico |
|---|---|---|---|---|
| Fijación simbiótica | \(N_2 \rightarrow NH_3\) | Rhizobium, Bradyrhizobium | Simbiosis con raíces de leguminosas, microaerofilia | Aporte directo de nitrógeno a plantas cultivadas |
| Fijación libre | \(N_2 \rightarrow NH_3\) | Azotobacter (aerobio), Clostridium (anaerobio) | Suelos, ambientes acuáticos, carbono orgánico disponible | Contribución difusa pero constante a la fertilidad natural |
| Nitrificación (paso 1) | \(NH_3 \rightarrow NO_2^-\) | Nitrosomonas, Nitrosospira | Aerobiosis estricta, pH neutro a ligeramente alcalino | Formación de nitritos, precursores de los nitratos |
| Nitrificación (paso 2) | \(NO_2^- \rightarrow NO_3^-\) | Nitrobacter, Nitrospira | Aerobiosis, tolerancia a un amplio rango de temperaturas | Producción de nitratos, forma altamente asimilable por las plantas |
| Desnitrificación | \(NO_3^- \rightarrow N_2\) (vía \(NO_2^-\), NO, \(N_2O\)) | Pseudomonas, Paracoccus, Bacillus | Anoxia (suelos saturados, sedimentos), materia orgánica lábil | Cierre del ciclo, retorno del \(N_2\) a la atmósfera |
| Amonificación (mineralización) | N orgánico \(\rightarrow NH_4^+\) | Hongos saprófitos (Bacillus, Streptomyces, etc.) | Aerobiosis o anaerobiosis, descomposición de necromasa | Reciclaje del nitrógeno a partir de residuos orgánicos |
N.B.: La actividad humana mediante fertilizantes sintéticos ha duplicado el flujo de nitrógeno reactivo que ingresa a los ecosistemas terrestres desde 1950.
Antes de la era industrial, los flujos naturales de fijación biológica y atmosférica mantenían un stock estable de nitrógeno reactivo en suelos y aguas. Los trabajos de Justus von Liebig (1803-1873) ya habían intuido la importancia de los compuestos nitrogenados para la fertilidad. Pero fue la invención del proceso Haber-Bosch (primera década del siglo XX) la que multiplicó la producción de fertilizantes nitrogenados sintéticos. Hoy, la fijación antropogénica supera a la fijación natural.
El exceso de nitratos lixiviados por la lluvia llega a los ríos y luego a las zonas costeras, causando zonas muertas eutróficas donde las proliferaciones de algas asfixian a la fauna acuática. El golfo de México o el mar Báltico ilustran esta contaminación difusa. Además, el óxido nitroso (\(N_2O\)), subproducto de la nitrificación y la desnitrificación, es un gas de efecto invernadero 300 veces más potente que el dióxido de carbono, contribuyendo al calentamiento global.
Es el conjunto de procesos que transforman el nitrógeno atmosférico en formas utilizables por los seres vivos y lo devuelven después a la atmósfera.
Porque la molécula N₂ es muy estable y solo ciertas bacterias pueden romperla.
Realizan las etapas clave: fijación, nitrificación, amonificación y desnitrificación.
Absorben nitratos y amonio del suelo para producir proteínas, aminoácidos y ADN.
Los fertilizantes, la contaminación y las emisiones industriales añaden demasiado nitrógeno reactivo, causando eutrofización y desequilibrios ecológicos.