

Parce que l’azote, indispensable à la construction des protéines et de l’ADN, ne peut être utilisé directement par la plupart des êtres vivants sous sa forme gazeuse pourtant abondante dans l’atmosphère. Le cycle de l’azote transforme continuellement cet élément, grâce à l’action combinée des bactéries, des plantes, des animaux et des phénomènes naturels, en formes assimilables par le vivant. Sans ces conversions successives — fixation, nitrification, assimilation, ammonification et dénitrification — les écosystèmes s’effondreraient rapidement. Ce cycle invisible mais fondamental maintient l’équilibre biologique de la planète et conditionne la fertilité des sols, la productivité des océans et la stabilité du climat.
L'atmosphère terrestre contient près de 78 % de diazote (\(N_2\)) en volume ou 75 % en masse. Pourtant, cette énorme ressource potentielle pour la vie est inaccessible à la grande majorité des êtres vivants. Aucun animal, aucun humain, aucune plante ne peut la transformer en nutriment.
La raison tient à la robustesse exceptionnelle de la triple liaison chimique entre les deux atomes d'azote (N≡N). Une énergie considérable est nécessaire pour rompre cette liaison.
Deux voies existent: l'éclair et ses 30 000 °C, ou l'élégance chimique des bactéries et leur enzyme nitrogénase, capable de réduire N₂ en NH₃ (diazote → ammoniac). Sans cette rupture préalable, pas de protéines, pas d'ADN, pas de muscles, pas de neurones, pas de sang: pas de vie.
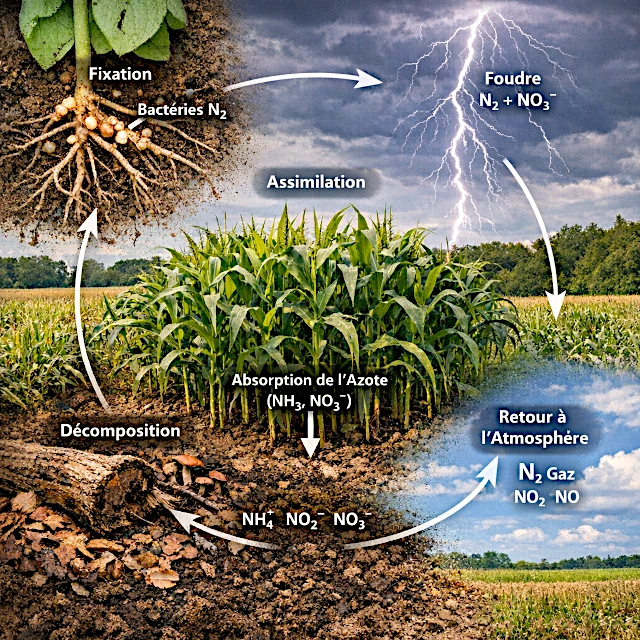
Le cycle de l'azote est une cascade de transformations qui convertit un gaz inerte en nutriments assimilables, puis le reconduit vers l'atmosphère.
N.B.: Antoine Lavoisier (1743-1794) proposa le terme « azote » (du grec « a‑zôê », sans vie). Paradoxalement, cet élément inerte sous forme gazeuse se révèle indispensable à toute cellule vivante dès qu'il est fixé.
| Processus | Transformation chimique | Bactéries + Champignons | Conditions requises | Rôle écologique |
|---|---|---|---|---|
| Fixation symbiotique | \(N_2 \rightarrow NH_3\) | Rhizobium, Bradyrhizobium | Symbiose avec racines de légumineuses, microaérophilie | Apport d'azote directement aux plantes cultivées |
| Fixation libre | \(N_2 \rightarrow NH_3\) | Azotobacter (aérobie), Clostridium (anaérobie) | Sols, milieux aquatiques, carbone organique disponible | Contribution diffuse mais constante à la fertilité naturelle |
| Nitrification (étape 1) | \(NH_3 \rightarrow NO_2^-\) | Nitrosomonas, Nitrosospira | Aérobiose stricte, pH neutre à légèrement alcalin | Formation de nitrites, précurseurs des nitrates |
| Nitrification (étape 2) | \(NO_2^- \rightarrow NO_3^-\) | Nitrobacter, Nitrospira | Aérobiose, tolérance à une large gamme de températures | Production de nitrates, forme hautement assimilable par les plantes |
| Dénitrification | \(NO_3^- \rightarrow N_2\) (via \(NO_2^-\), NO, \(N_2O\)) | Pseudomonas, Paracoccus, Bacillus | Anoxie (sols saturés, sédiments), matière organique labile | Refermeture du cycle, retour du \(N_2\) à l'atmosphère |
| Ammonification (minéralisation) | N organique \(\rightarrow NH_4^+\) | Champignons saprophytes (Bacillus, Streptomyces, etc.) | Aérobiose ou anaérobiose, décomposition de nécromasse | Recyclage de l'azote à partir des déchets organiques |
N.B.: L'activité humaine via les engrais de synthèse a doublé les flux d'azote réactif entrant dans les écosystèmes terrestres depuis 1950.
Avant l'ère industrielle, les flux naturels de fixation biologique et atmosphérique maintenaient un stock stable d'azote réactif dans les sols et les eaux. Les travaux de Justus von Liebig (1803-1873) avaient déjà pressenti l'importance des composés azotés pour la fertilité. Mais c'est l'invention du procédé Haber-Bosch (première décennie du 20e siècle) qui a démultiplié la production d'engrais azotés de synthèse. Aujourd'hui, la fixation anthropique dépasse la fixation naturelle.
L'excès de nitrates lessivés par les pluies gagne les rivières puis les littoraux, provoquant des zones mortes eutrophes où les proliférations d'algues asphyxient la faune aquatique. Le golfe du Mexique ou la mer Baltique illustrent cette pollution diffuse. Par ailleurs, l'oxyde nitreux (\(N_2O\)), sous-produit de la nitrification et de la dénitrification, est un gaz à effet de serre 300 fois plus puissant que le dioxyde de carbone, contribuant au réchauffement climatique.
C’est l’ensemble des transformations qui permettent à l’azote de passer de sa forme atmosphérique à des formes utilisables par le vivant, puis de retourner dans l’atmosphère.
Parce que les organismes ne peuvent pas casser la molécule N₂, très stable. Seules certaines bactéries sont capables de la fixer.
Elles assurent les étapes clés: fixation, nitrification, ammonification et dénitrification, rendant l’azote accessible ou le renvoyant dans l’atmosphère.
Elles absorbent les nitrates et ammoniums présents dans le sol pour fabriquer protéines, acides aminés et ADN.
Les engrais, la pollution et la combustion industrielle ajoutent trop d’azote réactif dans l’environnement, provoquant eutrophisation, déséquilibres écologiques et émissions de gaz à effet de serre.