

Et si la vie n'était ni le fruit d’une contingence ni celui d’une finalité, mais l’expression d’une transition de phase de la matière soumise à un flux d’énergie?
Comment, à partir de molécules inertes, la vie a-t-elle pu émerger sur Terre il y a ~3,8 milliards d'années? Cette interrogation peut être abordée sous un angle moderne en examinant le principe de cellule minimale. Il s’agit de déterminer quelle est la forme organisationnelle la plus élémentaire capable de conserver un état interne régulé face aux variations de l’environnement et de se reproduire de manière autonome.
Source: Des théories classiques comme celles de Alexander Oparin (1894-1980) et J.B.S. Haldane (1892-1964), proposaient que la vie pouvait émerger progressivement dans une "soupe primitive" d’éléments chimiques. Aujourd’hui, le concept de cellule minimale permet d’envisager la naissance du vivant comme la formation spontanée d’un système capable de maintenir un équilibre interne et de se reproduire, à partir de lois physiques et chimiques fondamentales.
La cellule moderne constituent l’unité fondamentale de tous les organismes vivants (bactéries, archées, eucaryotes). Cependant, même les cellules les plus simples, sont déjà des cathédrales moléculaires d'une complexité vertigineuse.
Chez l’homme, on estime que l’organisme contient environ 37 000 milliards de cellules, réparties en plus de 200 types cellulaires différents. Chaque type cellulaire possède des caractéristiques morphologiques et biochimiques spécifiques adaptées à ses fonctions biologiques.
Source: Selon Geoffrey H. Stoeckius et collaborateurs (2021), plus de 200 types cellulaires distincts ont été identifiés chez l’homme, chacun spécialisé pour des fonctions physiologiques précises. Théorie endosymbiotique (Lynn Margulis, 1967): Explication de l'origine des mitochondries et des chloroplastes par l'incorporation de bactéries dans des cellules eucaryotes.
La Terre primitive offrait une gigantesque expérimentation naturelle: des trillions de milliards de réactions chimiques menées simultanément se poursuivaient pendant des centaines de millions d'années. Chaque mare tiède, chaque fissure hydrothermale, chaque minéral poreux ou grain d'argile formait un laboratoire miniature où les molécules organiques pouvaient se rassembler. Constamment brassées par les cycles naturels sur des temps longs, ces molécules empruntaient progressivement les voies chimiques menant aux briques du vivant: acides aminés, sucres, lipides et bases de l'ARN.
N.B.:
Si les débats sur l'origine de la vie restent animés, un point fait consensus: les acides aminés, qui forment les protéines, constituent des briques moléculaires essentielles à tout organisme vivant. De plus, leur formation naturelle est possible dans l'espace car on en a trouvé dans les météorites. Cela suggère que les acides aminés étaient probablement disponibles sur la Terre primitive.
Source: Les conditions de la Terre primitive, avec ses sources hydrothermales, mares tièdes et minéraux catalytiques, ont été proposées comme "laboratoires naturels" pour la synthèse prébiotique par Stanley Miller (1930-2007) et Harold Urey (1953).
Les atomes sont en mouvement constant en raison de l’agitation thermique, qui provoque de légers déplacements et vibrations au sein des molécules. Les liaisons chimiques faibles, comme les ponts hydrogène et les interactions van der Waals (forces attractives ou répulsives), maintiennent ensemble les atomes dans les molécules primitives à base de carbone. Le carbone, grâce à ses 4 liaisons covalentes stables, est l’élément parfait pour construire des assemblages moléculaires.
Les vibrations aléatoires des molécules, se comportant comme de minuscules aimants électriques, permettent aux structures chimiques d'explorer simultanément différentes conformations spatiales. De nouvelles formes moléculaires sont créées continuellement, augmentant ainsi les chances des arrangements stables. Cette diversité constitue un réservoir virtuellement illimité de formes moléculaires, dont seules les structures électromagnétiquement stables persisteront assez longtemps pour être soumises à la sélection naturelle.
Source: Comme le montrent les travaux de Max Delbrück (1949) sur les fluctuations stochastiques dans les systèmes biologiques, ces mouvements aléatoires permettent aux structures chimiques de tester simultanément de nombreuses conformations. Auto-assemblage moléculaire: Travaux de Jean-Marie Lehn né en 1939 (chimie supramoléculaire) sur les interactions faibles (liaisons hydrogène, forces de van der Waals).
Certaines configurations moléculaires vont permettre l'auto-réplication naturelle qui repose sur un principe simple: la complémentarité structurale.
Une macromolécule (simple brin repliée en une forme 3D) agit comme un moule dont la forme et les charges électriques attirent précisément certains éléments chimiques libres présents autour d'elle. Ces éléments libres viennent s'aligner le long du brin selon leur compatibilité chimique pour former une deuxième chaîne complémentaire distincte (comme un négatif photographique). On obtient alors une structure à deux chaînes appariées, assemblée pièce par pièce à partir des composants environnants.
Les deux chaînes maintenues ensemble par des liaisons hydrogène finissent par se rompre naturellement, sous l'effet de l'agitation thermique du milieu. Cet équilibre énergétique est crucial car il faut suffisamment d'agitation pour permettre les rencontres et les séparations, mais pas trop pour préserver l'intégrité des structures assemblées (mares tièdes, sources hydrothermales, etc.). Cette macromolécule complémentaire peut elle-même servir de moule pour recréer la séquence initiale.
Par ce mécanisme purement physico-chimique (attraction → alignement → appariement → séparation → restitution de la séquence initiale) il devient possible de comprendre comment des macromolécules d'ARN capables de se répliquer ont pu émerger spontanément sur la Terre primitive.
Source: La réplication spontanée des molécules d'ARN s'inscrit dans le cadre de la théorie du monde à ARN, proposée par Walter Gilbert (1986), qui suggère que l'ARN pouvait à la fois stocker l'information et catalyser des réactions chimiques.
Le système devient auto-catalytique: certaines molécules d'ARN se répliquent plus vite que d'autres, en recrutant les nucléotides (A, G, C, U) libres plus efficacement. Les petites erreurs et variations créent de nouvelles formes, avec des vitesses de copie et des stabilités différentes. Les molécules les plus rapides et stables prolifèrent, les moins efficaces disparaissent. Cette sélection est naturelle et résulte directement des lois de la cinétique chimique dans un système hors équilibre c'est-à-dire agité et alimenté par un flux constant de matière.
Source: La dynamique de sélection auto-catalytique rappelle les modèles proposés par Eigen et Schuster (1977) sur les hypercycles, décrivant comment la compétition et la réplication favorisent certaines molécules dans des systèmes chimiques hors équilibre.
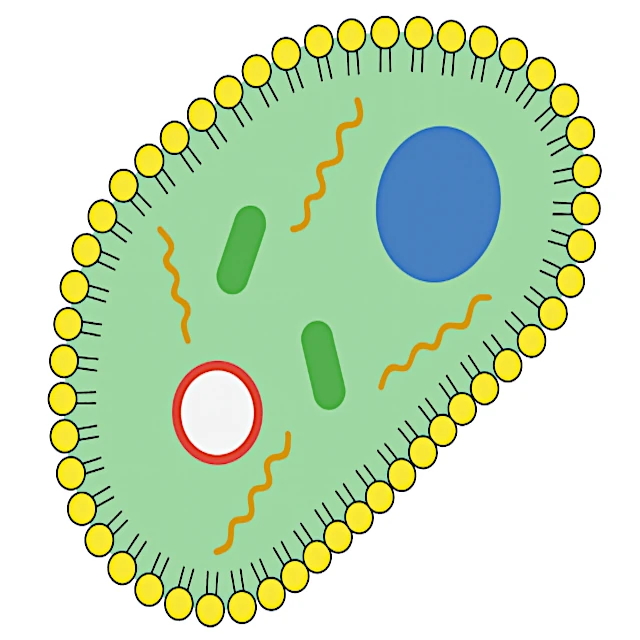
La transition des molécules réplicatives vers une véritable cellule nécessite l'apparition d'un compartiment membranaire. Les membranes biologiques sont constituées de phospholipides, de molécules amphiphiles qui s'organisent spontanément en bicouches lorsqu'elles sont en milieu aqueux. Cet auto-assemblage est naturel: il est thermodynamiquement favorable et se produit sans besoin d'intervention extérieure, un peu comme une bulle de savon qui se forme spontanément à la surface de l'eau.
Une protocellule protégée par une membrane lipidique et contenant des molécules d'ARN capables de se répliquer possède les caractéristiques essentielles d'un organisme vivant minimal. Elle dispose d'un métabolisme (production de ses propres composants internes), d'une capacité de reproduction (division cellulaire) et d'un support d'information transmissible (ARN). À partir de ce stade, l'évolution darwinienne peut pleinement opérer, favorisant les protocellules les plus efficaces pour croître et se diviser dans leur environnement.
Source: L'auto-assemblage des phospholipides en bicouches a été observé expérimentalement et est expliqué par la thermodynamique des systèmes amphiphiles (Bangham et al., 1965). Cela montre que la formation de membranes ne nécessite pas d’intervention biologique.