

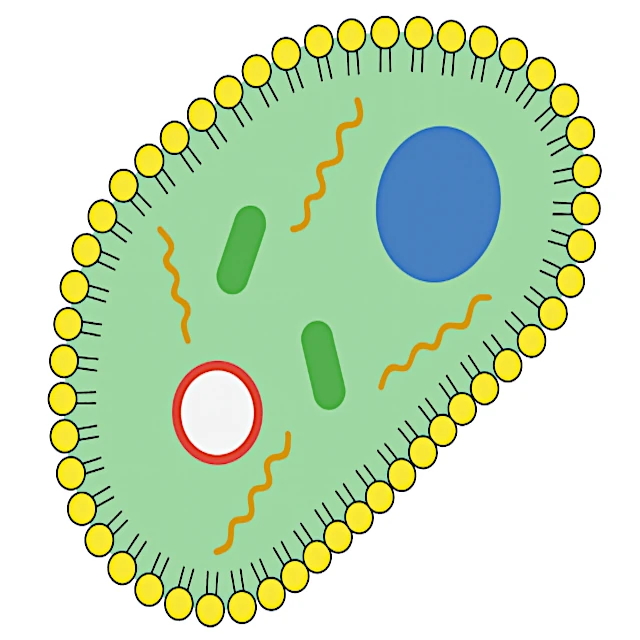
¿Y si la vida no fuera ni el fruto de una contingencia ni de una finalidad, sino la expresión de una transición de fase de la materia sometida a un flujo de energía?
¿Cómo, a partir de moléculas inertes, pudo emerger la vida en la Tierra hace ~3.800 millones de años? Esta interrogación puede abordarse desde un ángulo moderno examinando el principio de la célula mínima. Se trata de determinar cuál es la forma organizativa más elemental capaz de conservar un estado interno regulado frente a las variaciones del entorno y reproducirse de manera autónoma.
Fuente: Teorías clásicas de científicos como Alexander Oparin (1894–1980) y J.B.S. Haldane (1892–1964) proponían que la vida podía surgir gradualmente en una "sopa primitiva" de elementos químicos. Hoy, el concepto de célula mínima permite considerar el origen de la vida como la formación espontánea de un sistema capaz de mantener un equilibrio interno y reproducirse, a partir de leyes físicas y químicas fundamentales.
Las células modernas constituyen la unidad fundamental de todos los organismos vivos (bacterias, arqueas, eucariotas). Sin embargo, incluso las células más simples ya son catedrales moleculares de una complejidad vertiginosa.
En el ser humano, se estima que el organismo contiene unos 37 billones de células, repartidas en más de 200 tipos celulares diferentes. Cada tipo celular posee características morfológicas y bioquímicas específicas adaptadas a sus funciones biológicas.
Fuente: Según Geoffrey H. Stoeckius y colaboradores (2021), se han identificado más de 200 tipos celulares distintos en el ser humano, cada uno especializado en funciones fisiológicas específicas. Teoría endosimbiótica (Lynn Margulis, 1967): Explica el origen de las mitocondrias y los cloroplastos mediante la incorporación de bacterias en células eucariotas.
La Tierra primitiva ofrecía un experimento natural gigantesco: billones de reacciones químicas se llevaban a cabo simultáneamente durante cientos de millones de años. Cada charco cálido, cada fisura hidrotermal, cada mineral poroso o grano de arcilla formaba un laboratorio en miniatura donde las moléculas orgánicas podían reunirse. Constantemente agitadas por los ciclos naturales durante largos periodos, estas moléculas seguían gradualmente las vías químicas que conducen a los ladrillos de la vida: aminoácidos, azúcares, lípidos y bases del ARN.
N.B.:
Si los debates sobre el origen de la vida siguen siendo animados, hay un punto de consenso: los aminoácidos, que forman las proteínas, constituyen ladrillos moleculares esenciales para cualquier organismo vivo. Además, su formación natural es posible en el espacio, ya que se han encontrado en meteoritos. Esto sugiere que los aminoácidos probablemente estaban disponibles en la Tierra primitiva.
Fuente: Las condiciones de la Tierra primitiva, con sus fuentes hidrotermales, charcos cálidos y minerales catalíticos, fueron propuestas como "laboratorios naturales" para la síntesis prebiótica por Stanley Miller (1930–2007) y Harold Urey (1953).
Los átomos están en movimiento constante debido a la agitación térmica, que provoca pequeños desplazamientos y vibraciones dentro de las moléculas. Los enlaces químicos débiles, como los puentes de hidrógeno y las interacciones de van der Waals (fuerzas atractivas o repulsivas), mantienen unidos los átomos en las moléculas primitivas basadas en carbono. El carbono, gracias a sus 4 enlaces covalentes estables, es el elemento perfecto para construir ensamblajes moleculares.
Las vibraciones aleatorias de las moléculas, que se comportan como pequeños imanes eléctricos, permiten a las estructuras químicas explorar simultáneamente diferentes conformaciones espaciales. Se crean continuamente nuevas formas moleculares, aumentando así las posibilidades de arreglos estables. Esta diversidad constituye un reservorio virtualmente ilimitado de formas moleculares, de las cuales solo las estructuras electromagnéticamente estables persistirán el tiempo suficiente para ser sometidas a la selección natural.
Fuente: Como muestran los trabajos de Max Delbrück (1949) sobre las fluctuaciones estocásticas en los sistemas biológicos, estos movimientos aleatorios permiten a las estructuras químicas probar simultáneamente numerosas conformaciones. Autoensamblaje molecular: Trabajos de Jean-Marie Lehn (nacido en 1939) sobre química supramolecular, centrados en interacciones débiles (enlaces de hidrógeno, fuerzas de van der Waals).
Ciertas configuraciones moleculares permitirán la autorréplica natural, que se basa en un principio simple: la complementariedad estructural.
Una macromolécula (una hebra simple plegada en una forma 3D) actúa como un molde cuya forma y cargas eléctricas atraen con precisión ciertos elementos químicos libres presentes a su alrededor. Estos elementos libres se alinean a lo largo de la hebra según su compatibilidad química para formar una segunda cadena complementaria distinta (como un negativo fotográfico). Se obtiene entonces una estructura de dos cadenas apareadas, ensamblada pieza por pieza a partir de los componentes circundantes.
Las dos cadenas mantenidas juntas por enlaces de hidrógeno terminan por romperse naturalmente, bajo el efecto de la agitación térmica del medio. Este equilibrio energético es crucial, ya que se necesita suficiente agitación para permitir los encuentros y las separaciones, pero no demasiado para preservar la integridad de las estructuras ensambladas (charcos cálidos, fuentes hidrotermales, etc.). Esta macromolécula complementaria puede, a su vez, servir de molde para recrear la secuencia inicial.
Mediante este mecanismo puramente fisicoquímico (atracción → alineación → apareamiento → separación → restitución de la secuencia inicial), es posible comprender cómo las macromoléculas de ARN capaces de replicarse pudieron emerger espontáneamente en la Tierra primitiva.
Fuente: La replicación espontánea de las moléculas de ARN se enmarca en la teoría del mundo de ARN, propuesta por Walter Gilbert (1986), que sugiere que el ARN podía tanto almacenar información como catalizar reacciones químicas.
El sistema se vuelve autocatalítico: ciertas moléculas de ARN se replican más rápido que otras, reclutando los nucleótidos libres (A, G, C, U) de manera más eficiente. Los pequeños errores y variaciones crean nuevas formas, con diferentes velocidades de copia y estabilidades. Las moléculas más rápidas y estables proliferan, mientras que las menos eficaces desaparecen. Esta selección es natural y resulta directamente de las leyes de la cinética química en un sistema fuera de equilibrio, es decir, agitado y alimentado por un flujo constante de materia.
Fuente: La dinámica de selección autocatalítica recuerda a los modelos propuestos por Eigen y Schuster (1977) sobre los hiperciclos, que describen cómo la competencia y la replicación favorecen ciertas moléculas en sistemas químicos fuera del equilibrio.
La transición de las moléculas replicativas a una verdadera célula requiere la aparición de un compartimento de membrana. Las membranas biológicas están compuestas por fosfolípidos, moléculas anfipáticas que se organizan espontáneamente en bicapas cuando están en un medio acuoso. Este autoensamblaje es natural: es termodinámicamente favorable y se produce sin necesidad de intervención externa, algo así como una burbuja de jabón que se forma espontáneamente en la superficie del agua.
Una protocélula protegida por una membrana lipídica y que contiene moléculas de ARN capaces de replicarse posee las características esenciales de un organismo vivo mínimo. Dispone de un metabolismo (producción de sus propios componentes internos), una capacidad de reproducción (división celular) y un soporte de información transmisible (ARN). A partir de este estadio, la evolución darwiniana puede operar plenamente, favoreciendo a las protocélulas más eficaces para crecer y dividirse en su entorno.
Fuente: El autoensamblaje de fosfolípidos en bicapas ha sido observado experimentalmente y se explica mediante la termodinámica de los sistemas anfifílicos (Bangham et al., 1965). Esto demuestra que la formación de membranas no requiere intervención biológica.