

Die Erdatmosphäre enthält fast 78 % Distickstoff (\(N_2\)) nach Volumen oder 75 % nach Masse. Dennoch ist diese riesige potenzielle Ressource für das Leben für die meisten Lebewesen unzugänglich. Kein Tier, kein Mensch, keine Pflanze kann ihn in Nährstoffe umwandeln.
Der Grund liegt in der außergewöhnlichen Stärke der dreifachen chemischen Bindung zwischen den beiden Stickstoffatomen (N≡N). Es ist beträchtliche Energie erforderlich, um diese Bindung zu brechen.
Es gibt zwei Wege: der Blitz mit seinen 30.000 °C oder die chemische Eleganz der Bakterien und ihres Enzyms Nitrogenase, das \(N_2\) zu \(NH_3\) reduzieren kann (Distickstoff → Ammoniak). Ohne diesen vorherigen Bruch gäbe es keine Proteine, keine DNA, keine Muskeln, keine Neuronen, kein Blut: kein Leben.
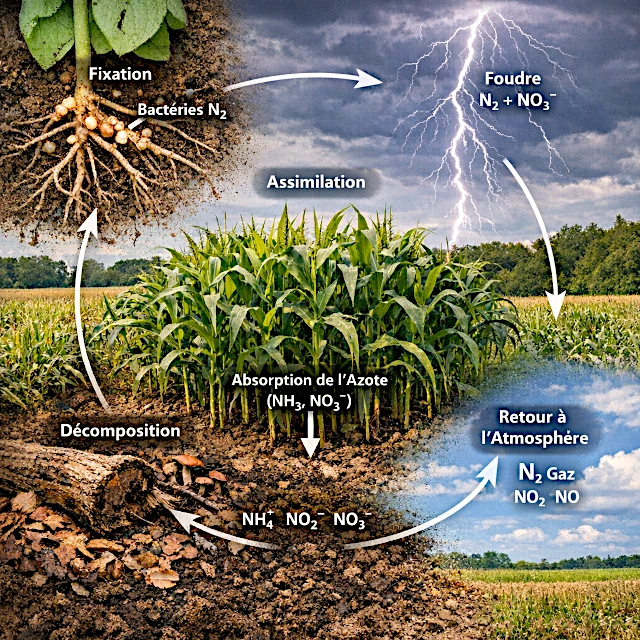
Der Stickstoffkreislauf ist eine Kaskade von Umwandlungen, die ein inertes Gas in assimilierbare Nährstoffe umwandelt und es dann in die Atmosphäre zurückführt.
N.B.: Antoine Lavoisier (1743-1794) schlug den Begriff "Stickstoff" (von griechisch "a-zôê", ohne Leben) vor. Paradoxerweise erweist sich dieses in Gasform inerte Element als unverzichtbar für jede lebende Zelle, sobald es fixiert ist.
| Prozess | Chemische Umwandlung | Bakterien + Pilze | Erforderliche Bedingungen | Ökologische Rolle |
|---|---|---|---|---|
| Symbiotische Fixierung | \(N_2 \rightarrow NH_3\) | Rhizobium, Bradyrhizobium | Symbiose mit Leguminosenwurzeln, Mikroaerophilie | Direkte Stickstoffversorgung für Kulturpflanzen |
| Freie Fixierung | \(N_2 \rightarrow NH_3\) | Azotobacter (aerob), Clostridium (anaerob) | Böden, aquatische Umgebungen, verfügbarer organischer Kohlenstoff | Diffuse, aber konstante Beitrag zur natürlichen Fruchtbarkeit |
| Nitrifikation (Schritt 1) | \(NH_3 \rightarrow NO_2^-\) | Nitrosomonas, Nitrosospira | Strikte Aerobiose, neutraler bis leicht alkalischer pH-Wert | Bildung von Nitriten, Vorläufer von Nitraten |
| Nitrifikation (Schritt 2) | \(NO_2^- \rightarrow NO_3^-\) | Nitrobacter, Nitrospira | Aerobiose, Toleranz gegenüber einem breiten Temperaturbereich | Produktion von Nitraten, hoch assimilierbare Form für Pflanzen |
| Denitrifikation | \(NO_3^- \rightarrow N_2\) (über \(NO_2^-\), NO, \(N_2O\)) | Pseudomonas, Paracoccus, Bacillus | Anoxie (gesättigte Böden, Sedimente), labile organische Substanz | Schließung des Kreislaufs, Rückkehr von \(N_2\) in die Atmosphäre |
| Ammonifikation (Mineralisierung) | Organischer N \(\rightarrow NH_4^+\) | Saprophytische Pilze (Bacillus, Streptomyces, etc.) | Aerobiose oder Anaerobiose, Zersetzung von Nekromasse | Recycling von Stickstoff aus organischen Abfällen |
N.B.: Die menschliche Aktivität durch synthetische Düngemittel hat den Fluss von reaktivem Stickstoff, der seit 1950 in terretrische Ökosysteme gelangt, verdoppelt.
Vor dem Industriezeitalter hielten die natürlichen Flüsse der biologischen und atmosphärischen Fixierung einen stabilen Bestand an reaktivem Stickstoff in Böden und Gewässern aufrecht. Die Arbeiten von Justus von Liebig (1803-1873) hatten bereits die Bedeutung von Stickstoffverbindungen für die Fruchtbarkeit erahnt. Doch die Erfindung des Haber-Bosch-Verfahrens (erstes Jahrzehnt des 20. Jahrhunderts) vervielfachte die Produktion von synthetischen Stickstoffdüngern. Heute übersteigt die anthropogene Fixierung die natürliche Fixierung.
Überschüssige Nitrate, die durch Regen ausgwaschen, gelangen in Flüsse und dann in Küstengebiete, wo sie eutrophe Tote Zonen verursachen, in denen Algenblüten die aquatische Fauna ersticken. Der Golf von Mexiko oder die Ostsee veranschaulichen diese diffuse Verschmutzung. Darüber hinaus ist Distickstoffmonoxid (\(N_2O\)), ein Nebenprodukt der Nitrifikation und Denitrifikation, ein Treibhausgas, das 300-mal wirksamer ist als Kohlendioxid und zur globalen Erwärmung beiträgt.