

O nitrogénio é indispensável para a formação de proteínas e ADN, mas a maioria dos seres vivos não consegue utilizá-lo na sua forma gasosa, apesar de ser abundante na atmosfera. O ciclo do nitrogénio converte continuamente este elemento em formas assimiláveis graças à ação de bactérias, plantas, animais e processos naturais. Sem essas transformações, os solos perderiam fertilidade, os oceanos a sua produtividade e os ecossistemas entrariam em colapso. Este ciclo invisível, mas fundamental, mantém o equilíbrio biológico do planeta.
A atmosfera terrestre contém cerca de 78% de dinitrogênio (\(N_2\)) em volume ou 75% em massa. No entanto, esse enorme recurso potencial para a vida é inacessível à grande maioria dos seres vivos. Nenhum animal, humano ou planta pode transformá-lo em nutrientes.
A razão está na robustez excepcional da ligação química tripla entre os dois átomos de nitrogênio (N≡N). Uma energia considerável é necessária para romper essa ligação.
Existem duas vias: o raio e seus 30.000 °C, ou a elegância química das bactérias e sua enzima nitrogenase, capaz de reduzir \(N_2\) a \(NH_3\) (dinitrogênio → amônia). Sem essa ruptura prévia, não haveria proteínas, nem DNA, nem músculos, nem neurônios, nem sangue: não haveria vida.
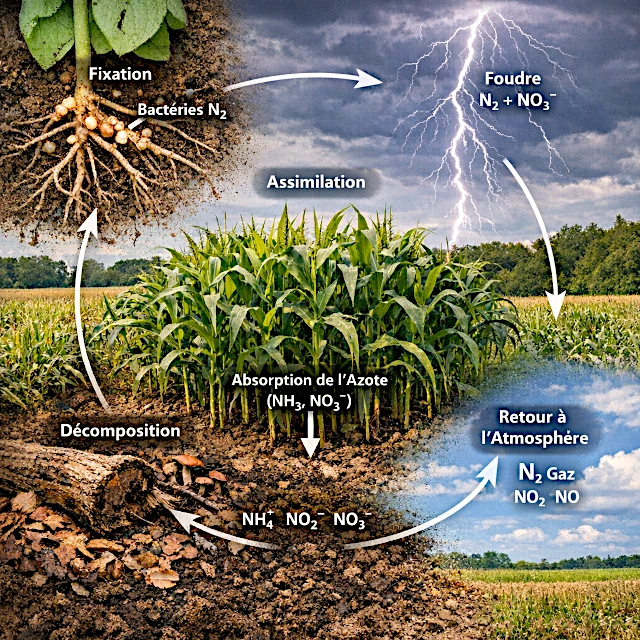
O ciclo do nitrogênio é uma cascata de transformações que converte um gás inerte em nutrientes assimiláveis, depois o reconduz à atmosfera.
N.B.: Antoine Lavoisier (1743-1794) propôs o termo "nitrogênio" (do grego "a-zôê", sem vida). Paradoxalmente, esse elemento inerte em forma gasosa revela-se indispensável a toda célula viva assim que fixado.
| Processo | Transformação química | Bactérias + Fungos | Condições necessárias | Papel ecológico |
|---|---|---|---|---|
| Fixação simbiótica | \(N_2 \rightarrow NH_3\) | Rhizobium, Bradyrhizobium | Simbiose com raízes de leguminosas, microaerofilia | Fornecimento direto de nitrogênio para plantas cultivadas |
| Fixação livre | \(N_2 \rightarrow NH_3\) | Azotobacter (aeróbio), Clostridium (anaeróbio) | Solos, ambientes aquáticos, carbono orgânico disponível | Contribuição difusa, mas constante, para a fertilidade natural |
| Nitrificação (etapa 1) | \(NH_3 \rightarrow NO_2^-\) | Nitrosomonas, Nitrosospira | Aerobiose estrita, pH neutro a levemente alcalino | Formação de nitritos, precursores dos nitratos |
| Nitrificação (etapa 2) | \(NO_2^- \rightarrow NO_3^-\) | Nitrobacter, Nitrospira | Aerobiose, tolerância a uma ampla faixa de temperaturas | Produção de nitratos, forma altamente assimilável pelas plantas |
| Desnitrificação | \(NO_3^- \rightarrow N_2\) (via \(NO_2^-\), NO, \(N_2O\)) | Pseudomonas, Paracoccus, Bacillus | Anoxia (solos saturados, sedimentos), matéria orgânica lábil | Fechamento do ciclo, retorno do \(N_2\) à atmosfera |
| Amonificação (mineralização) | N orgânico \(\rightarrow NH_4^+\) | Fungos saprófitos (Bacillus, Streptomyces, etc.) | Aerobiose ou anaerobiose, decomposição de necromassa | Reciclagem do nitrogênio a partir de resíduos orgânicos |
N.B.: A atividade humana por meio de fertilizantes sintéticos dobrou o fluxo de nitrogênio reativo que entra nos ecossistemas terrestres desde 1950.
Antes da era industrial, os fluxos naturais de fixação biológica e atmosférica mantinham um estoque estável de nitrogênio reativo nos solos e nas águas. Os trabalhos de Justus von Liebig (1803-1873) já haviam pressentido a importância dos compostos nitrogenados para a fertilidade. Mas foi a invenção do processo Haber-Bosch (primeira década do século XX) que multiplicou a produção de fertilizantes nitrogenados sintéticos. Hoje, a fixação antropogênica supera a fixação natural.
O excesso de nitratos lixiviados pela chuva atinge os rios e depois as zonas costeiras, causando zonas mortas eutróficas onde a proliferação de algas asfixia a fauna aquática. O golfo do México ou o mar Báltico ilustram essa poluição difusa. Além disso, o óxido nitroso (\(N_2O\)), subproduto da nitrificação e da desnitrificação, é um gás de efeito estufa 300 vezes mais potente que o dióxido de carbono, contribuindo para o aquecimento global.
É o conjunto de processos que convertem o nitrogénio atmosférico em formas utilizáveis pelos seres vivos e o devolvem à atmosfera.
Porque a molécula N₂ é muito estável e apenas certas bactérias conseguem quebrá-la.
Elas realizam as etapas essenciais: fixação, nitrificação, amonificação e desnitrificação.
Absorvem nitratos e amónio do solo para formar proteínas, aminoácidos e ADN.
Fertilizantes, poluição e emissões industriais adicionam nitrogénio reativo em excesso, causando eutrofização e desequilíbrios ecológicos.