

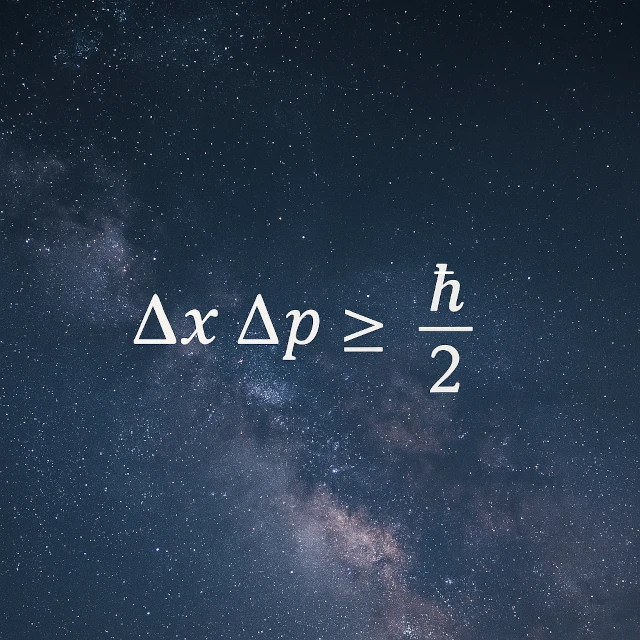
El principio de incertidumbre de Heisenberg (Δx × Δp ≥ ħ/2) afirma que es imposible conocer simultáneamente con precisión la posición (Δx) y el momento lineal (Δp) de una partícula cuántica. Cuanto más se conoce la posición, menos se conoce su velocidad, y viceversa. Si una partícula estuviera inmóvil, significaría que su posición (fija) y su momento (cero) estarían perfectamente determinados, violando esta desigualdad. A escala cuántica (por ejemplo, para un electrón en un átomo), confinar una partícula en un espacio pequeño le confiere automáticamente movimiento: la inmovilidad es, por tanto, imposible.
La fórmula de Einsenberg es un descubrimiento fundamental de la mecánica cuántica. Formulada en 1927 por Werner Einsenberg (1901-1976), expresa un límite fundamental a la precisión con la que ciertas parejas de propiedades físicas, como la posición (x) y la cantidad de movimiento (p), pueden ser conocidas simultáneamente.
Esta relación se expresa matemáticamente por la desigualdad: Δx * Δp ≥ ħ/2, donde \(\hbar = \frac{h}{2\pi}\) (h = constante de Planck y ħ = constante de Planck reducida). La desigualdad (≥) significa que el producto de las dos incertidumbres (Δx) y (Δp) nunca puede descender por debajo de ħ/2.
En otras palabras: Cuanto más precisamente se mide la posición de una partícula (Δx), menos precisamente se puede conocer su cantidad de movimiento (Δp), y viceversa. Este es un límite fundamental de la naturaleza, no una limitación técnica de nuestros instrumentos. Nunca podemos conocer simultáneamente y con precisión absoluta la posición y la velocidad de una partícula cuántica.
Δx (delta x) representa la incertidumbre en la posición de una partícula. Es el "margen de error" o la imprecisión con la que conocemos exactamente dónde se encuentra la partícula en el espacio. Δp (delta p) representa la incertidumbre en la cantidad de movimiento (o impulso) de la partícula. La cantidad de movimiento p = mv (masa × velocidad), por lo que Δp mide la imprecisión en la velocidad/movimiento de la partícula. El producto Δx * Δp representa, por lo tanto, el producto de estas dos incertidumbres.
ħ (h-barra) es la constante de Planck reducida, igual a h/2π, donde h es la constante de Planck (aproximadamente 1,054 × 10⁻³⁴ J·s). Es una constante fundamental de la naturaleza que caracteriza la escala cuántica. ħ/2 es, por lo tanto, la mitad de esta constante.
La pequeña magnitud de ħ no significa que a nuestra escala macroscópica "conozcamos" la posición y el movimiento de un objeto. Significa que nuestras imprecisiones de medición habituales son enormes en comparación con ħ/2, enmascarando así los efectos cuánticos de los objetos macroscópicos. La desigualdad siempre se verifica ampliamente en la práctica.
A escala cuántica, nuestras precisiones de medición son del orden de 10⁻¹⁵ m, muy lejos de ħ/2. Lo que cambia es que el compromiso impuesto por ħ/2 se vuelve relevante para comprender el comportamiento de las partículas. El principio de incertidumbre se vuelve físicamente significativo a esta escala porque confinar un electrón en un espacio de 10⁻¹⁰ m (tamaño de un átomo) implica automáticamente que tiene movimiento, y reducir Δx obliga a aumentar Δp según la relación ΔxΔp ≥ ħ/2.
Un electrón inmóvil y localizado es, por lo tanto, imposible, lo que explica por qué ninguna partícula puede estar en reposo.
Imagina que intentas tomar una foto muy nítida de un coche que circula a gran velocidad. Para obtener una imagen nítida, debes usar un tiempo de exposición muy corto. Sin embargo, un tiempo de exposición corto significa que captas menos luz, lo que puede hacer que la imagen quede oscura o borrosa si la luz es insuficiente.
Δx (delta x) representa la incertidumbre en la posición de la partícula. Δp (delta p) representa la incertidumbre en su momento lineal (masa × velocidad). Su producto nunca puede ser inferior a ħ/2, donde ħ es la constante de Planck reducida (aproximadamente 1,054 × 10⁻³⁴ J·s). Este límite es fundamental: no proviene de un defecto de nuestros instrumentos, sino de la naturaleza intrínseca del mundo cuántico.
Sí, pero sus efectos son totalmente imperceptibles a nuestra escala. La constante ħ es extremadamente pequeña. Para un objeto macroscópico, las imprecisiones de medida habituales son enormes comparadas con ħ/2, por lo que la desigualdad siempre se cumple ampliamente. Solo a escala cuántica (átomos, electrones, fotones) el compromiso impuesto por ħ/2 se vuelve físicamente significativo y determina el comportamiento de las partículas.
Tiene varias consecuencias importantes: muestra que la realidad cuántica es intrínsecamente probabilística (reemplazando el determinismo clásico). Explica la cuantificación de la energía en átomos y moléculas. Es fundamental para el efecto túnel (una partícula atraviesa una barrera de energía clásicamente infranqueable), utilizado en transistores y microscopios de efecto túnel. Implica que el vacío cuántico nunca está perfectamente vacío, sino sujeto a fluctuaciones, y está íntimamente ligado a la dualidad onda-partícula.